为了测定某有机物A的结构,做如下实验: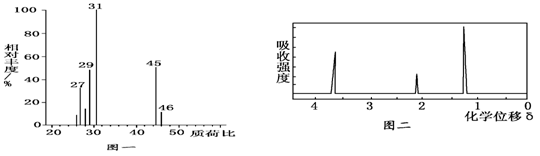
①将9.2g该有机物完全燃烧,生成0.4 mol CO2和10.8 g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1∶2∶3.试回答下列问题:
(1)有机物A的相对分子质量是________.(2)有机物A的实验式是________.
(3)能否根据A的实验式确定A的分子式________(填“能”或“不能”),若能,则A的分子式是________(若不能,则此空不填).(4)写出有机物A可能的结构简式_______.
(1)0.1 mol某烃在足量的氧气中完全燃烧,生成的CO2和水各0.6 mol,则该烃的分子式为。
(2)若该烃不能使溴水或高锰酸钾溶液褪色,但在一定条件下,可以和液溴发生取代反应,其一溴取代物只有一种,则此烃属于烃,结构简式为,名称是,该烃的二 氯代物有种。
(3)若该烃能使溴水褪色,且能在催化剂作用下与H2发生加成反应,生成2,2—二甲基丁烷,则此烃属于烃,结构简式为, 名称是;
核磁共振氢谱有个吸收峰,其面积比是。
下列物质中,与该烃互为同系物的是(填序号)_________,互为同分异 构体的是________。
① CH3CH===CHCH3 ② CH2===CHC(CH3)3
③ CH3CH2CH===CHCH2CH3 ④(CH3)2CH(CH2)2CH3
化合物A(C11H8O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B和C。回答下列问题:
⑴B的分子式为C2H4O2,分子中只有一个官能团。则B的结构简式是________,B与乙醇在浓硫酸催化下加热反应生成D,该反应的化学方程式是______________________,该反应的类型是________;写出两种能发生银镜反应的B的同分异构体的结构简式__________________________。
⑵C是芳香化合物,相对分子质量为180,其碳的质量分数为60.0%,氢的质量分数为4.4%,其余为氧,则C的分子式是_____________。
⑶已知C的芳环上有三个取代基,其中一个取代基无支链,且还有能使溴的四氯化碳溶液褪色的官能团及能与碳酸氢钠溶液反应放出气体的官能团,则该取代基上的官能团名称是。另外两个取代基相同,分别位于该取代基的邻位和对位,则C的结构简式是。
⑷A的结构简式是。
W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为_____________________。
(2)W与Y可形成化合物W2Y,该化合物的电子式为___________________________。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为___________。
(4)比较Y、Z气态氢化物的稳定性:___________>___________。(用分子式表示)
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是________(用元素符号表示)。
(6)Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量。写出该反应的热化学方程式:_____________________________。
一定条件下,在体积为3 L的密闭容器中有反应:
CO(g)+2H2(g) 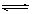 CH3OH(g) (催化剂为Cu2O/ZnO),根据题意完成下列各题:
CH3OH(g) (催化剂为Cu2O/ZnO),根据题意完成下列各题: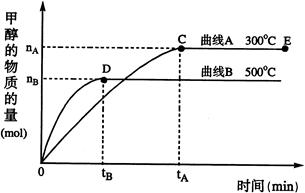
(1)反应达到平衡时,平衡常数表达式K=,升高温度,K值 (填“增大”、“减小”或“不变”);
(2)在500℃,从反应开始到平衡,H2的平均反应速率v(H2)=(用nB、tB表示);
(3)下列描述中能说明上述反应已达平衡的是;
a.v(CO)=2v(H2)
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(4)开始向密闭容器中充入0.10 molCO和0.20 molH2,一段时间后达到平衡,测得容器中CH3OH物质的量为0.08 mol;若再通入0.10 molCO和0.20 molH2,则平衡移动 (填“正向”、“逆向”或“不”);若平衡移动,再次达到平衡后,mol<n(CH3OH)<mol。
日常生活中的塑料包括很多种,其中PET(聚对苯二甲酸乙二醇酯)塑料被广泛用于生产包装瓶、电器元件、汽车配件等;PS塑料被广泛应用于光学工业中,PET塑料、PS塑料可按下图所示合成。
(1)C能与含氧酸发生酯化反应,则C的分子式为,其所含的官能团的名称为。
(2)X、Y互为同分异构体,分子式为C8H10,则X的结构简式为,
其核磁共振氢谱有种峰。
(3)D分子中含有一个甲基,则D→E的化学方程式为,
E与CH2=CH—CH=CH2在一定条件下1︰1发生反应生成除苯环外无支链的高聚物的化学方程式为。
(4)Z是B的同分异构体,其具有如下性质:①遇FeCl3溶液显紫色;②能与NaHCO3溶液反应放出CO2;③苯环上的一氯代物只有三种;④苯环上只有2个取代基相邻。则Z的结构最多有种,写出其中一种的结构简式。