(8分)某研究性学习小组为了制取氨气和探究氨气的有关性质,进行了下列实验。
(1)根据图A氨气的制备装置制取氨气,试回答:制取氨气的化学反应方程式
___________ ____;收集氨气的方法是______________ __
(2)甲、乙两组同学用干燥的圆底烧瓶各收集一瓶氨气,根据图B喷泉实验的装置进行实验,都观察到美丽的红色喷泉。
根据实验现象说明氨气具有的性质是____________________________________;
(3)甲、乙两组同学完成喷泉实验后,圆底烧瓶中所得溶液如图C所示。请通过分析确认:甲组同学所得氨水的物质的量浓度_______(填“大于”、“小于”或“等于”)乙组同学所得氨水的物质的量浓度。
(1)某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
①写出A中有机反应的化学方程式 。
②已知上述有机反应是放热反应,观察到A中的现象是:_____ 及 _________。
③实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
④C中盛放CCl4的作用是 。
⑤能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中滴入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入______ _____,现象是______________________。
(2)乙炔的实验室制法
①反应原理_____ ____________。
②选择合适的制取实验装置___ ___。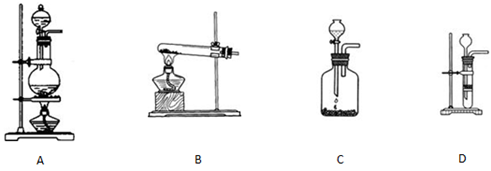
③实验中常用饱和食盐水代替水,目的是______ __________。
④纯净的乙炔气体是无色无味的气体,用电石和水反应制取的乙炔,常含有H2S和PH3而有恶臭气味。可以用____ _______溶液除去杂质气体。
实验室制备溴苯可用如图所示装置。
请回答下列问题:
(1)关闭F夹,打开C夹,在装有少量苯的三口烧瓶中由A口加入液Br2,再加入少量铁屑,塞住A口,则三口烧瓶中发生反应的化学方程式为:
和 。
(2)试管D、E内出现的现象依次为 、 。
(3)待三口烧瓶中的反应进行到仍有气泡冒出时打开F夹,关闭C夹,可以看到的现象是 。(可多选)
A.甲中的水倒吸入乙中
B.甲中有大量气泡冒出
C.乙中的溶液进入甲中
D.乙中溶液出现分层现象
(4)若要除去溴苯中混有的Br2,可选择试剂_________。
A.酒精B.NaOH溶液C.CCl4D.苯
下图为苯和溴的取代反应的改进实验装置图。其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入铁屑粉少量。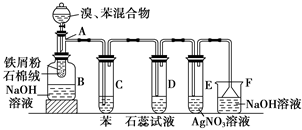
填写下列空白:(注:溴苯与NaOH溶液不可以发生水解反应)
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):
________________________________________________________________________
________________________________________________________________________。
(2)试管C中苯的作用是_________;反应开始后,观察D和E试管,看到的现象为:D中:________;
E中:___________________________ ______。
(3)反应2 min至3 min后,在B中的NaOH溶液可观察到的现象是____________________。
(4)在上述整套装置中,具有防倒吸的仪器有________(填字母)。
(5)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这3个优点外,还有一个优点是:________________________________。
用A、B、C三种装置都可制取溴苯,请仔细分析三套装置,然后回答下列问题:
(1)写出三个装置中都发生反应的化学方程式 、 ;写出B试管中发生反应的化学方程式 。
(2)装置A、C中长导管的作用是 。
(3)B、C装置已连接好,并进行了气密性检验,也装入了合适的药品,接下来要使反应开始,对B应进行的操作是 ,
对C应进行的操作是 。
(4)A中存在加装药品和及时密封的矛盾,因而在实验中易造成的不良后果是 。
(5)B中采用了双球吸收管,其作用是 ;反应后双球管中可能出现的现象是 ;双球管内液体不能太多,原因是 。
(6)B装置也存在两个明显的缺点,使实验的效果不好或不能正常进行,这两个缺点是 。
为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验:
将一定量的苯和溴放在烧瓶中,同时加入少量铁屑,3~5 min后发现装有AgNO3溶液的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应。
(1)装置I中①的化学方程式为____________________,___________________。
(2)①中长导管的作用是________________________________________________。
(3)烧瓶中生成的红褐色油状液滴的成分是__________________________,要想得到纯净的产物,可用____________试剂洗涤。洗涤后分离产品应使用的仪器是_______________。
(4)甲做实验时,乙观察到烧瓶中液体沸腾并有红棕色气体从导管中逸出,提出必须先除去红棕色气体,才能验证锥形瓶中的产物,原因是_____________________________。
(5)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验。可选用的试剂是:苯;液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳。
a的作用是___________________________________
b中的试剂是_________________________________
比较两套装置,装置Ⅱ的主要优点是:(答出两点即可)
①____________________________________________
②____________________________________________