①在实验室里,要证明钠、镁、铝的金属性依次减弱的实验,除钠、镁、铝以外,还需的试剂为_________________________。
②在实验室里,要做证明Cl、Br、I的非金属性依次减弱的实验,所需的试剂除:NaCl溶液,NaBr溶液,KI溶液外,还需要的试剂为____________________。
反应的离子方程式为:_______________________________________________________
__________ ______________ __________________
________ ____
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化亚铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)ΔH>0
2Fe(s)+3CO2(g)ΔH>0
①该反应的平衡常数表达式为:K=
②该温度下,在2L盛有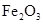 粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为
粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为
(2)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)
和温度(T)的关系示意图中与铝热反应最接近的是。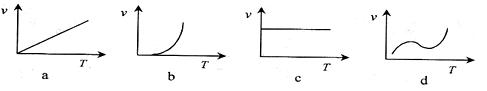
(3)Fe3+盐和Al3+盐在性质上有很多相似的地方,如遇碱都生成难溶的胶状沉淀,可用于净水;也有不同之处,如Fe3+既有氧化性又有还原性,Al3+只有氧化性。但Fe3+只有在碱性介质中才能被氧化为FeO42-,请完成下列方程式:
Fe(OH)3 +ClO- + ==FeO42- + Cl- +;
(4)若将ag Fe和Al的混合物溶于2mol/L的足量的硫酸中,再往溶液中加入足量的6mol/L的NaOH溶液,充分反应,过滤,洗涤,干燥灼烧,称量所得固体的质量仍为ag,则原混合物中Al的质量分数为
自洁面料就是在普通的面料纤维中加入一层薄薄的纳米二氧化钛。含有Fe2O3的钛铁矿(主要成分为FeTiO3,Ti的最高价为 +4)制取纳米级TiO2的流程如下:
+4)制取纳米级TiO2的流程如下: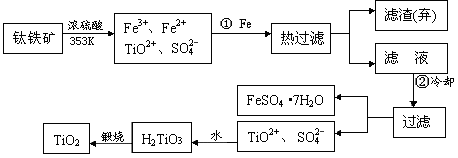
(1)步骤①发生的主要反应是_________________(用离子方程式表示)
(2)上述制备二氧化钛的过程中,可以利用的副产物是______________;考虑成本和废物综合利用因素,废液中应加入___________________处理。
(3)由金红石制备单质钛,涉及到的步骤为:
TiO2 TiCl4
TiCl4 Ti
Ti
已知:①C(s)+O2(g)=CO2(g)△H=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g)△H=+141.0kJ·mol-1
则TiO2(s)+ 2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H=____________ kJ·mol-1
反应TiCl4+2Mg =2MgCl2+Ti 在氩气氛中进行的理由是________________________。
(4)TiO2是白色粉末,不溶于水,也不溶于酸,但能溶于氢氟酸和热的浓硫酸中。请写出TiO2与硫酸反应的方程式
Ⅰ.短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中X、Y、Z三种元素的质子数之和为21。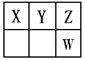
(1)写出W的简单离子的原子结构示意图;
氢元素与Z形成原子个数比为1∶1的化合物,其结构式为。
(2)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是(用离子方程式表示);
(3)写出Y的最高价氧化物对应水化物的浓溶液与X在加热条件下反应的化学方程式 ,
,
反应中每转移8mol 电子,消耗的还原剂质量为g。
(4)写出能说明Y的非金属性比Z弱的一个实验事实:
Ⅱ.往1L体积不变的容器中加入0.200mol CO和1.00mol H2O(g),在t℃时反应:
CO+ H2O(g)  CO2+ H2达到平衡,若该反应的化学平衡常数K=1,则t℃时CO 的转化率为。
CO2+ H2达到平衡,若该反应的化学平衡常数K=1,则t℃时CO 的转化率为。
Ⅲ.甲醇燃料电池是一种相对理想的绿色能源,可用于电动汽车的电源;若该氢氧燃料电池以硫酸为电解质溶液,总反应为:2CH3OH + 3O2 = 2CO2+ 4H2O,则其正极的电极反应式
(12分)合成氨对化学工业和国防工业具有重要意义。
⑴向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图。
①图A中氨气的体积分数为15%时,H2的转化率为。
②图B中T=500℃,则温度为450℃时对应的曲线是(填“a”或“b”)。
⑵合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为CH4(g)+H2O(g)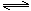 CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表: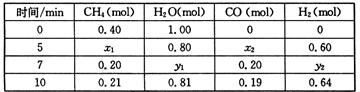
①分析表中数据,判断5 min时反应是否处于平衡状态? (填“是”或“否”),
前5 min反应的平均反应速率v(CH4)=。
②该温度下,上述反应的平衡常数K=。
③反应在7~10 min内,CO的物质的量减少的原因可能是(填字母)。
a.减少CH4的物质的量 b.降低温度 c.升高温度d.充入H2
(10分)下图是一些常见的单质和化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为生活中最常用的金属单质,J为红褐色固体,L为两性氢氧化物。反应①、②均为工业上的重要反应。
请回答下列问题:
⑴写出B的化学式为;D的电子式为。
⑵组成单质C的元素在元素周期表中的位置为;
⑶写出向I溶液中加入过量NaOH溶液时发生反应的离子方程式:
。
⑷写出向Na2SiO3溶液中通入少量D时发生反应的离子方程式:
。