化学活动小组的同学用下图所示装置进行实验(装置的气密性良好):先关闭止水夹,将足量氢氧化钠溶液滴入锥形瓶中,充分反应后,再打开止水夹。
(1)锥形瓶中能观察到的现象是 ;
(2)探究反应后锥形瓶内溶液中溶质成份的几种可能情况:对其成分他们分别做出了如下猜想:
甲同学猜想可能含有NaOH和Ca(OH)2 ;乙同学猜想可能含有NaOH、Na2CO3和Ca(OH)2
丙同学猜想可能恰好完全反应只含NaOH ;丁同学猜想可能含有 。
你认为甲、乙、丙同学的猜想都合理吗?哪位同学猜想是错误的,请分析原因是
[物质鉴别]化学小组同学选用了两种不同类别的试剂进行实验,鉴别甲同学猜想,并得出结论——氢氧化钙存在。请将鉴别的化学方程式填在下表中。
| |
化 学 方 程 式 |
| 试剂1 |
|
| 试剂2 |
|
某化学兴趣小组获得两包制作"跳跳糖"的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末。将少量柠檬酸和这种白色粉末溶于水,混合后产生了使澄清石灰水变浑浊的气体,为确定白色粉末的化学成分,进行了以下探究:
【提出猜想】猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.碳酸钠和碳酸氢钠。
【查阅资料】①碳酸钠溶液、碳酸氢钠溶液均呈碱性;
②碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;碳酸钠受热不分解。
【实验探究1】小亮、小刚分别对有关猜想设计方案并进行实验:
|
实验操作 |
实验现象 |
实验结论 |
|
|
小亮 |
将白色粉末溶于水后用pH试纸测定其酸碱度 |
pH 7(填">"、"<"或"=") |
溶液呈碱性,猜想1成立 |
|
小刚 |
用右图所示的装置进行实验 |
试管A中有水珠产生,试管B中液体变浑浊 |
猜想2成立,试管B中反应的化学方程式为 |
【实验质疑】
(1)小红认为小亮的实验结论不正确,理由是 。(用文字叙述)
(2)小明认为小刚的实验并不能得出猜想2成立,理由是 。(用文字叙述)
【实验探究2】为了进一步确定白色粉末的化学成分,小戚称取10g白色粉末与足量稀盐酸反应,充分反应后生成二氧化碳的质量为m g,通过计算并分析实验数据确定猜想3成立,则m的取谊范围为 (计算结果用分数表示)。
【结论分析】探究后他们查到该白色粉末的成分为碳酸氢钠,那么你认为白色粉末中的碳酸钠是如何产生的?写出产生碳酸钠的化学方程式 。

现有一瓶标签破损的白色固体(如图),化学兴趣小组的同学们决定对该白色固体成分进行实验探究。
【提出问题】这瓶白色固体的成分是什么?
【查阅资料】氯化钠,硫酸钠,硝酸钠的溶液是中性。
【做出猜想】猜想1 氯化钠 猜想2 氢氧化钠 猜想3 碳酸钠 猜想4…………
【实验探究】为了证明猜想,同学们取白色固体置于烧杯中,加水配成溶液,进行如下实验探究:
|
实验步骤 |
实验现象 |
实验结论 |
|
(1)取少量溶液于试管中,滴加酚酞溶液 |
酚酞溶液变红 |
说明溶液呈 性, 猜想1不成立 |
|
(2)取少量溶液于试管中,滴加稀盐酸 |
有气泡生成,气体通入澄清石灰水,石灰水变浑浊 |
猜想2 (填"成立"或"不成立") |
|
(3)取少量溶液于试管中,滴加氯化钙溶液 |
试管中 |
猜想3不成立 |
【讨论交流】实验后,同学们找老师交流探讨,请教之后得出这瓶白色固体是 。
【拓展】为了进一步验证结论,同学们在老师指导下,有做了该物质受热分解的实验,确定结论正确。

聪聪做镁条在空气中燃烧实验时发现除生成白色固体外还有少量淡黄色固体,他对得到的固体成分进行探究。
【提出问题】固体成分是什么?
【提出猜想】猜想一:MgO
猜想二:Mg 3N 2
猜想三:
【查阅资料】MgO与水反应类似于CaO与水反应;Mg 3N 2与水反应产生NH 3。
|
实验操作 |
实验现象 |
实验结论 |
|
将该固体投入到盛水的烧杯中 |
若烧杯中只有白色固体,无刺激性气味气体产生 |
猜想 正确 |
|
|
猜想二或猜想三正确 |
【表达与交流】聪聪在老师的指导下,用定量的方法确定猜想三正确,请写出将固体投入水中相关反应的化学方程式。 、 。
【相关结论】空气中N 2和O 2体积比约为 ,由镁条在空气中燃烧生成少量Mg 3N 2可得出的一个结论是 。
小红同学将氢氧化钠和氢氧化钙的溶液分别加入试管A、B中,进行了如图所示的三组实验。根据实验Ⅰ、Ⅱ、Ⅲ逐步完成下列问题:
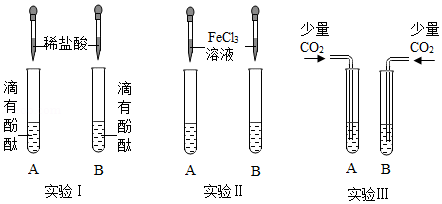
(1)小红设计的实验Ⅰ,证明酸和碱能发生中反应,写出稀盐酸和氢氧化钙溶液发生的化学方程式 。
(2)实验Ⅱ中,针对反应现象,可总结出碱溶液的化学通性之一是 。
(3)实验Ⅲ,B中有白色沉淀生成,A中无现象。为确定通入CO 2后A中溶质的成分,小红进行了如下探究:
【提出猜想】
猜想a。溶质只有氢氧化钠
猜想b。溶质只有碳酸钠
猜想c。溶质有氢氧化钠和碳酸钠
【实验与结论】
|
实验操作 |
实验现象 |
结论 |
|
①取A中溶液少量于试管中,逐滴滴加澄清石灰水 |
产生白色沉淀 |
猜想c成立 |
|
②待①中反应恰好完全时静置,取上层清液少许于试管中,滴加几滴酚酞溶液 |
溶液呈红色 |
【反思与评价】
教师评价小红得出的结论不正确,因为猜想 (选填"a"或"b")也有相同的现象。如果要验证"猜想c"成立,需将上述实验中的 换成 溶液。
小明在做"盐酸中和氢氧化钠"的实验时,实验前忘记向氢氧化钠溶液中滴加酚酞溶液,导致无法判断中和反应进行的程度,于是小明对反应后溶液的酸碱性进行了探究。
【探究目的】确定反应后溶液的酸碱性
【猜想与假设】反应后溶液呈碱性,也可能呈 ,也可能呈 。
【实验验证】
|
实验操作 |
实验现象 |
实验结论 |
|
|
无色酚酞溶液 ; |
溶液呈碱性,使其呈碱性的微粒是 ; |
|
无色酚酞溶液不变色 |
溶液呈 ; |
【继续验证】
|
实验操作 |
实验现象 |
实验结论 |
|
|
粉末部分或全部消失,溶液变为黄色 |
溶液呈 ,反应的化学方程式是 ; |
|
|
溶液呈 ; |