电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,
实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X电极上的电极反应是 ,
在X极附近观察到的现象是 。
②Y电极上的电极反应 ,
检验该电极反应产物的方法是 。
(2)若X和Y仍均为惰性电极,a为CuSO4溶液,则电解时的化学反应方程式为_____
_________________________。通过一段时间后,向所得溶液中加入16gCuO粉末,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为__________。
(3)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是___________,电极反应式是_________________________。
②Y电极的材料是___________,电极反应式是_________________________。
(说明:杂质发生的电极反应不必写出)
A. 海底热液研究(图1)处于当今科研的前沿。海底热液活动区域“黑烟囱”的周围常存在FeS、黄铜矿及锌矿等矿物。
(1) Ni2+的核外电子排布式是____________________。
(2) 分析下表,铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,基主要原因是 。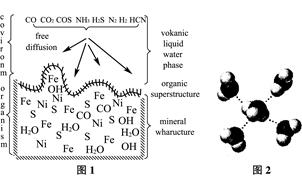
| 电离能/kJ·mol-1 |
I1 |
I2 |
| 铜 |
746 |
1958 |
| 锌 |
906 |
1733 |
(3) 下列说法正确的是________。
A. 电负性:N>O>S>C B. CO2与COS(硫化羰)互为等电子体
C. NH3分子中氮原子采用sp3杂化 D. CO、H2S、HCN都是极性分子
(4) “酸性热液”中大量存在一价阳离子,结构如图2,它的化学式为________________。
(5) FeS与NaCl均为离子晶体,晶胞相似,前者熔点为985℃,后者801℃,其原因是____________________________________________。在FeS晶胞中,与Fe2+距离相等且最近的S2-围成的多面体的空间构型为________________。
B. 制备KNO3晶体的实质是利用结晶和重结晶法对KNO3和NaCl的混合物进行分离。下面是某化学兴趣小组的活动记录:
| NaNO3 |
KNO3 |
NaCl |
KCl |
|
| 10℃ |
80.5 |
20.9 |
35.7 |
31.0 |
| 100℃ |
175 |
246 |
39.1 |
56.6 |
查阅资料:文献中查得,四种盐在不同温度下的溶解度(S/g)如下表:
实验方 案:
案:
Ⅰ. 溶解:称取29.8g KCl和34.0g NaNO3放入250mL烧杯中,再加入70.0g蒸馏水,加热并搅拌,使固体全部溶解。
Ⅱ. 蒸发结晶:继续加热和搅拌,将溶液蒸发浓缩。在100℃时蒸发掉50.0g水,维持该温度,在保温漏斗(如图所示)中趁热过滤析出的晶体。得晶体m1g。
Ⅲ. 冷却结晶:待溶液冷却至室温(实验时室温为10℃)后,进行减压过滤。得KNO3粗产品m2g。
Ⅳ. 重结晶:将粗产品全部溶于水,制成 100℃的饱和溶液,冷却至室温后抽滤。得KNO3纯品。
100℃的饱和溶液,冷却至室温后抽滤。得KNO3纯品。
假定:① 盐类共存时不影响各自的溶解度;② 各种过滤操作过程中,溶剂的损耗忽略不计。试回答有关问题:
(1) 操作Ⅱ中趁热过滤的目的是 。
(2) 若操作Ⅱ中承接滤液的烧杯中不加入蒸馏水,则理论上在操作Ⅲ中可得粗产品的质量m2=______g,其中混有NaCl______g。为防止NaCl混入,在操作Ⅱ中承接滤液的烧杯中至少应加入蒸馏水______g。
(3) 操作Ⅲ中采用减压过滤,其优点是______________________________________。该小组同学所用的装置如右图所示,试写出该装置中主要用到的玻璃仪器的名称:________________。若实验过程中发现倒吸现象,应采取的措施是______________________________________。
拉氧头孢钠是一种抗生素,合成拉氧头孢钠的中间体G的路线如下: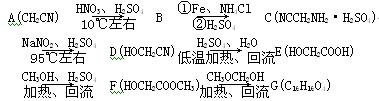
(1) B的结构简式为____________________。
(2) E―→F的反应类型为________________。
(3) 酚的苯环上某些氢原子比较活泼。由E合成F时还可能生成一种相对分子持量为194的副产物H,H的结构简式为______________________。
(4) M是E的同分异构体,M具有以下特征:① 苯环上只有2个取代基;② 遇氯化铁显色,但与小苏打不反应;③ 1mol M最多能与2mol NaOH溶液反应。则M的结构有________种。
(5) G含有酯基,请写出F―→G的化学反应方程式: 。
(6) 写出由化合物E制备化合物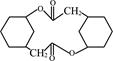 的合成路线流程图(无机试剂任选)。合成路线流程图示例:
的合成路线流程图(无机试剂任选)。合成路线流程图示例: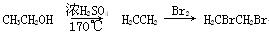
环己烷()在负载纳米Au的分子筛(Au/TS1)催化剂的作用下与空气发生氧化反应,反应原理是:通过游离基反 应形成环己基过氧化氢,该过氧化物在Au/TS1催化作用下受热分解,生成环己醇和环己酮(O)。由于环己醇、环己酮比环己烷更容易被氧化,因而有许多副产物(如己二酸及一些酯类化合物)生成。
应形成环己基过氧化氢,该过氧化物在Au/TS1催化作用下受热分解,生成环己醇和环己酮(O)。由于环己醇、环己酮比环己烷更容易被氧化,因而有许多副产物(如己二酸及一些酯类化合物)生成。
(1) 下表是某反应温度下,环己烷催化氧化反应的转化率(x)和目标产物的选择性(S)的结果:
| 催化剂 |
转化率(x)/% |
|||
| 目标产物的选择性(S)/% |
||||
| 环己基过氧化氢 |
环己醇 |
环己酮 |
||
| Au/TS1 |
10.4 |
14.1 |
34.9 |
39.8 |
① 写出环己烷催化氧化为环己酮的化学方程式: 。
② 若在反应容器中加入1.0mol环己烷,则生成的环己酮的物质的量为________(保留2位小数)。
(2) 图甲是反应温度对环己烷催化氧化反应的转化率(x)和目标产物的选择性(S)和目标产物的总收率(y)的影响。
① 由图甲可知:该反应较适宜的反应温度为________左右。
② 随着反应温度的升高,环己烷的转化率(x)逐渐增加,而目标产物的选择性(S)和 目标产物的总收率(y)却逐渐降低,其可能的原因是 。
目标产物的总收率(y)却逐渐降低,其可能的原因是 。
(3) 图乙是反应时间对环己烷催化氧化反应的转化率(x)和目标产物的选择性(S)和目标产物的总收率(y)的影响。
① 由图乙可知,该反应较适宜的反应时间为________左右。
② 随着反应时间的延长,环己烷的转化率(x)逐渐增加,而目标产物的选择性(S)逐渐降低,这说明________________________________________________________。
在探索生命奥妙的过程中,科学家们日益认识到生命细胞的组成和元素周期律有密切的关系。已知:①人体中不含稀有气体元素;②约占人体总质量99.97%的11种宏量元素,除K、Ca外,其余都为短周期元素;③其余0.03%是由十多种人体不可缺少的微量元素组成。在微量元素中,只有F和Si位于短周期,其余均在第一长周期。请根据试题要求,在11种宏量元素的8种元素中(除H、N、P外),选择合适元素填空:
(1)有一种元素A,其原子最外层电子数是内层电子数的2倍。则A处于元素周期表的位置为。
(2)有一种元素B,它的最高价氧化物对应的水化物是已知酸中酸性最强的酸,该酸的化学式为。宏量元素C是一种非金属元素,它与B处于同一周期,则C的原子结构示意图为。
(3)所有宏量元素中,元素D金属性最强 ,则D为(填元素符号)。除钙元素外,元素E也与D相邻。则E的单质与水反应的离子方程式为。
,则D为(填元素符号)。除钙元素外,元素E也与D相邻。则E的单质与水反应的离子方程式为。
(4)除A—E和钙元素外,还有两种宏量元素F、G。已知它们的离子的电子层结构相同,且带电量也相同但符号相反。F、G的离子中,半径较大的是(填离子符号)。
一切植物中均含有天然有机高分子化合物A,它是构成植物细胞壁的基础物质,不溶于水,也不溶于一般有机溶剂。能发生如下变化(A-F均分别代表一种物质,框图中的部分产物已略去)
|

