(I)将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置。试回答下列问题: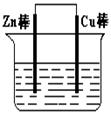
(1)若电解质溶液为稀硫酸,则Zn棒为原电池的 极,可观察到Cu棒上产生现象是 ,试用电极反应式表示该现象: 。
(2)若电解质为硫酸铜溶液,则Cu棒上发生 反应(填“氧化”“还原”),Zn棒上发生反应的电极反应式为: 。
(3)若在上述两个过程中,Zn棒减少的质量相等,则Cu棒上(1)和(2)所析出物质的质量之比为: 。
(II)A、B、C三个烧杯中分别盛有500mL相同物质的量浓度的稀硫酸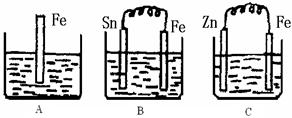
(1)写出A中离子反应方程式:
(2)一段时间后,B中Sn极附近溶液的pH (填“增大”、“减小”、“不变”)。
(3)一段时间后,C中产生了5.6L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度为
(4)反应完成后三个烧杯中液体质量大小顺序为:A B C (用<、=、>连接)。
工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺线路如下: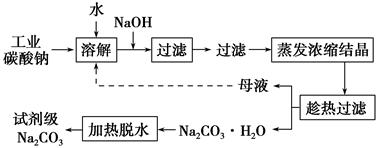
Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
Ⅱ.有关物质的溶度积如下:
| 物质 |
CaCO3 |
MgCO3 |
Ca(OH)2 |
Mg(OH)2 |
Fe(OH)3 |
| Ksp |
4.96×10-9 |
6.82×10-6 |
4.68×10-6 |
5.61×10-12 |
2.64×10-39 |
回答下列问题:
(1)加入NaOH溶液时发生反应的离子方程式为:_____________________________________。
向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=________。
(2)“趁热过滤”时的温度应控制在________。
(3)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用。请你分析实际工业生产中是否可行________,并说明理由________________________________________。
(4)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g)ΔH=+473.63 kJ·mol-1
写出NaCO3·H2O脱水反应的热化学方程式________________________________________。
以黄铁矿为原料,采用接触法生产硫酸的流程可简示如下: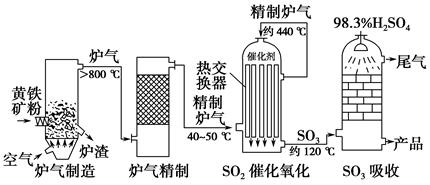
请回答下列问题:
(1)在炉气制造中,生成SO2的化学方程式为_________________________________________;
(2)炉气精制的作用是将含SO2的炉气________、________及干燥,如果炉气不经过精制,对SO2催化氧化的影响是___________________________________________;
(3)精制炉气(含SO2体积分数为7%、O2为11%、N2为82%)中SO2平衡转化率与温度及压强关系如下图所示。在实际生产中,SO2催化氧化反应的条件选择常压、450 ℃左右(对应图中A点),而没有选择SO2转化率更高的B或C点对应的反应条件,其原因分别是____________、____________;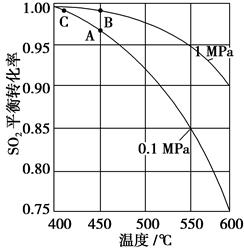
(4)在SO2催化氧化设备中设置热交换器的目的是________、________,从而充分利用能源。
工业上用粗氧化铜(含杂质FeO)为原料制取氯化铜晶体(CuCl2·2H2O)的生产流程如下: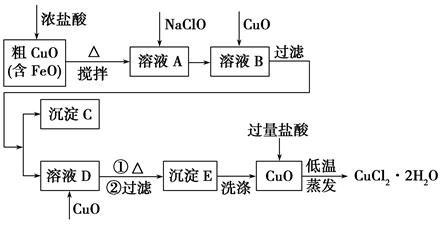
| 物质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| 完全沉淀时的pH |
≥9.6 |
≥6.4 |
3~4 |
(1)写出向溶液A中加入NaClO的离子方程式___________________________________。
(2)沉淀C的化学式为________。
(3)实验室如何检验沉淀E已洗涤干净?________。
(4)低温蒸发的目的是______________________________________。
(5)流程中两次加入了CuO,而不是一次性向溶液B中加入过量的CuO,其理由是________________________________________________。
分析以下两个案例,回答后面问题。
(1)某城镇生产、生活的分布情况如图所示,河流中W、X、Y、Z处某次水样抽测结果如表所示。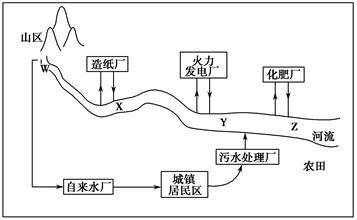
| 地点 项目 |
W |
X |
Y |
Z |
| 水温/℃ |
15 |
18 |
26 |
25 |
| pH |
6 |
8 |
5 |
5 |
| 溶解氧量/(mg·L-1) |
11 |
9 |
7 |
3 |
①导致X、Y处水样pH变化的原因可能是______________________________;
②Z处鱼类大量减少,产生这种现象的原因可能是_________________________。
(2)某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3、还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。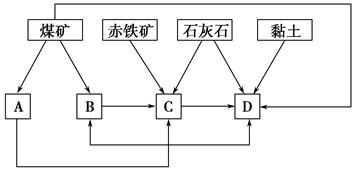
①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定上图中相应工厂的名称A________、B________、C________、D________;
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式_____________________________________________________________;
③从“三废”利用、环境保护等角度考虑,该地区和企业在生产中应采取的一些措施有____________(列举2种即可)。
以合成氨工厂工艺流程如下图,试回答相关问题: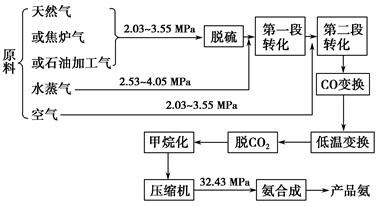
(1)不同的原料生产氢气其经济指标如下表:
| 天然气 |
石脑油 |
重油 |
煤焦 |
|
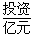 |
5.6 |
6.5 |
8.0 |
- |
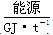 |
28~30 |
35.5 |
41.8 |
54.4 |
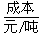 |
257 |
390~447 |
220~280 |
500 |
从上表数据及自然资源来看最具发展前景的是________。
A.天然气B.石脑油C.重油 D.煤焦
(2)脱硫工艺一般是通过金属氧化物来实现的,通过三步反应最后再生成金属氧化物,并得到单质硫,请补充第三步反应。
①MezOy+zH2S+(y-z)H2=MezSz+yH2O
②MezSz+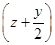 O2=MezOy+zSO2
O2=MezOy+zSO2
③__________________________________________________
(3)气体的精制 经净化过的气体仍有少量的CO等有害气体。常用的方法有铜洗法和甲烷化法。CO(g)+Cu(NH3)2Ac+NH3(l)[Cu(NH3)3CO]Ac;正反应放热,反应在铜洗塔中进行,吸收后的铜液送到再生器中,在再生器处解吸CO,适宜条件是________,解吸后铜液循环使用。甲烷化法则是把CO、CO2转化为对氨合成无害的CH4,主要反应是CO(g)+3H2(g) CH4(g)+H2O(g);正反应放热,甲烷化的条件是__________________。
CH4(g)+H2O(g);正反应放热,甲烷化的条件是__________________。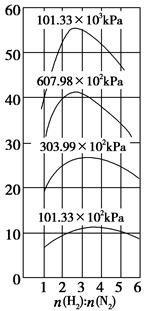
(4)500 ℃时,y随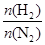 及压强的变化关系。纵坐标可能是____________,结合目前生产的条件,应控制的
及压强的变化关系。纵坐标可能是____________,结合目前生产的条件,应控制的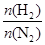 是________。
是________。