. 核磁共振谱是测定有机物分子结构最有用的工具之一。瑞士科学家维特里希等三人即是利用核磁共振技术测定生物大分子的三维结构而获得2002年诺贝尔化学奖。在有机物分子中,不同位置的氢原子在核磁共振氢谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目。例如:乙醛的结构式为: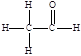 ,其PMR谱中有2个信号峰,其强度之比为3∶1。
,其PMR谱中有2个信号峰,其强度之比为3∶1。
⑴下列有机物分子中,在核磁共振氢谱中只给出一种峰(信号)的是( )
| A.CH3-CH3 | B.CH3OCH3 | C.CH3CH2OH | D.CH3CH2Cl |
⑵化合物A和B的分子式都是C2H4Br2,A的PMR谱上只有1个峰,则A的结构简式为 。
B的PMR谱上有 个峰,强度比为
(3)化合物分子式是C8H10,含苯环,其多种同分异构体中有一种在PMR谱上只有3个信号峰,强度比为3:1:1,其结构简式为 。
现有含NaCl、Na2SO4、Na2CO3和NaHCO3的固体混合物。某同学为测定其中各组分的含量,取部分样品溶于水,并设计了如下实验流程(所加试剂均为过量,反应①~③均为复分解反应)。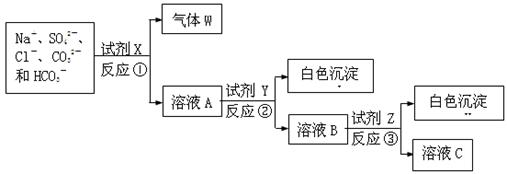
请回答: (1)气体W的化学式是。
(1)气体W的化学式是。
(2)反应①的离子方程式是 。
。
(3)试剂X、Y、Z依次是。
(4)下列说法正确的是(填字母) 。
。
a.溶液A的焰色反应为黄色
b.反应②和③之后均需进行过滤操作
c.若测得气体W的体积(标准状况)、白色沉淀Ⅰ和Ⅱ的质量,可计算出各组分的量
实验室欲配制500mL 0.5mol/L的NaOH溶液,有以下仪器:
(1)实验中需要称量NaOH 固体的质量是 。
(2)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为(填序号)____________________________。
(3)在配制过程中,如果没有洗涤烧杯和玻璃棒,其他操作都正确的,那么所配溶液的实际浓度将(填大于、小于或等于)0.5mol/L 。
现有下列4种物质:① NH3、② SO2、③ NaHCO3、④ Ca(ClO)2。其中,受热分解产生CO2的是(填序号,下同);遇氯化氢产生白烟的是;能使湿润的蓝色石蕊试纸变红的是;可由氯气与冷的消石灰反应制得的是。
某品牌番茄牛肉面的部分原料如下:① 食盐、② 牛肉、③ 西红柿、④ 小麦粉。请回答:
(1)富含淀粉的是(填序号,下同)。
(2)富含维生素的是。
(3)富含蛋白质的是。
(4)属于调味剂的是。
在3种有机物 ① 油脂、② 葡萄糖、③ 蛋白质中,遇浓硝酸变黄的是(填序号,下同),能发生皂化反应的是,能与新制氢氧化铜反应生成砖红色沉淀的是。