(9分)短周期的五种主族元素A、B、C、D、E原子序数依次变小。A的单质在常温下为气态,B、D属于同一主族,C为自然界含量最多的金属元素,D的最外层电子数为次外层的2倍,E为周期表中原子半径最小的元素。
(1)A、B的元素名称分别为 、 。
(2)D、E可以形成多种化合物,其中一种化合物的相对分子质量为28。写出其结构简
式 。
(3)自然界中B元素多以氧化物的形式存在,请写出工业上制取B单质的化学方程式
。
(4)写出实验室制取A气体的化学方程式 。
(5)a克C单质和氧化铁的混合物分为两等份,向其中一份中加入足量NaOH溶液,测得生成气体(标况,下同)体积为mL;另一份在高温下恰好完全反应,将产物冷却后加入足量HCl溶液,测得生成气体体积为nL。则m:n= 。
(9分)将反应IO3-+5I-+6H+ 3I2+3H2O设计成如图所示的原电池。
3I2+3H2O设计成如图所示的原电池。
(1)开始时向甲烧杯中加入少量浓硫酸,电流计指针向右偏转,此时甲池中发生的电极反应式为____________,工作过程中关于电流计的读数,下列说法正确的是_______(填编号)
a.电流计读数逐渐减小b.电流计读数有可能变为0
c.电流计读数一直不变d.电流计的读数逐渐增大
(2)如果在加浓硫酸前,甲、乙烧杯中都加入淀粉溶液,则溶液变蓝的烧杯是_______(填“甲”、“乙”)。
(3)工作一段时间后,如果再向甲烧杯滴入浓NaOH溶液,此时乙池中发生的电极反应式为____________,电流计指针向_____(填“左”、“右”)偏转。
(6分)按要求回答下列问题
(1)已知反应:mA(g) + nB(g)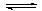 pC(g) + qD(g),v(A):v(B)= _________________;
pC(g) + qD(g),v(A):v(B)= _________________;
(2)任何情况下判断水溶液呈中性的依据是:_______________;
(3)NH4Cl溶液中离子浓度由大到小的顺序是:_________________。
(6分)完成下列离子反应方程式
(1)AlCl3溶液与Na2CO3溶液混合:____________;
(2)向AgCl固体上滴加Na2S溶液,固体变黑色:_________________;
(3)铁在潮湿的空气中发生电化腐蚀时,正极反应式:_________________。
(9分)下图是一套电解装置,两U型管中均盛有50.0 mL电解质溶液,a、b、c、d为 Pt电极。通电一段时间,d电极上析出金属Ag 2.16 g,没有气体产生。同时在b、c两极收集到标准状况下相同体积的气体。请回答:
(1)c为______极,写出c电极上的电极反应式:_______________,c极收集到的气体体积在标准状况下为___________L。
(2)b为______极,写出b电极上的电极反应式:开始时是____________、后来_______________。
(3)原CuCl2溶液中溶质的物质的量浓度为___________mol/L。
(7分)下图是铜锌原电池装置。其电池的总反应是:Zn(s) + CuSO4(aq)="=" ZnSO4(aq) + Cu(s)。
请回答以下问题:
(1)R的名称是____________,其作用是_____________。R中的阳离子移向_______(填A或B)中的溶液。
(2)电极Y的材料是________,B中的电解质溶液是______________。
(3)X为原电池的______极,其电极反应式是______________________。