用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下: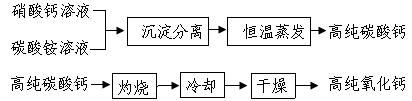
(1)写出下列物质的化学式:硝酸钙__________、碳酸铵___________。
(2)硝酸钙与碳酸铵在溶液中反应,其基本反应类型为___________。
(3)实验室常采用______________操作进行沉淀分离。
(4)生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是:
________________________________________________________。
(5)高纯氧化钙生产过程中,“干燥”的主要目的是为了防止(用化学方程式表示)
________________________________________________________。
硝酸钾是初中化学常见的一种盐。请按要求填写下列有关空格:
(1)质量分数为4.04%的硝酸钾溶液可作为番茄无土栽培的营养液。该营养液(填 "属于"或"不属于")复合肥。硝酸钾中含有的离子是、(填符号)。
(2)黑火药爆炸的反应原理是::
。此反应的反应物和生成物中,没有涉及到下列物质类别中的(填序号)。
| A. | 单质 | B. | 氧化物 | C. | 酸 | D. | 碱 E.盐 |
(3)下图为硝酸钾和氯化钠两种物质的溶解度曲线示意图,其中曲线(填"a"或"b")表示
的溶解度随温度变化的趋势。欲将接近饱和的
溶液变成饱和溶液,可采取的方法有、(列举两种)。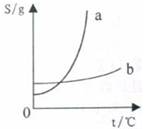
(4)在硝酸钾中,质量分数最大的元素是。
风和日丽的假日,同学们相约去湖边烧烤。
(1)小黄采购食物时,已购买了土豆、牛肉、虾和黄油,就营养均衡的角度而言,还应采购(填字母);
| A. | 鲫鱼 | B. | 青椒 | C. | 鸡翅 | D. | 面包 |
(2)小赵生火时,发现火柴不能直接将干燥的木炭点燃,为顺利生火,可采取的措施是:
;
(3)小李烧烤时尽量避免烤焦食物,因为烤焦的食物中常含苯并芘(
)等多种有害物质。苯并芘中碳元素的质量分数约为%(保留一位小数);
(4)小谭清洗餐具时使用了洗洁精,利用其作用将餐具洗得更洁净;
(5)烧烤结束,灭火时发现,少量水浇在炽热的木炭上,火焰反而更大,这是由于此时生成了一氧化碳和氢气,写出该反应的化学方程式:。
012年6月,"蛟龙"号载人潜水器创造了我国载人深潜新纪录,实现了我国深海技术发展的重大跨越。
(1)蛟龙"号身披能抗超高压的钛合金"龙甲"。钛合金属于材料,它的硬度(填"小于"或"大于")金属钛的硬度;
(2)下潜时,载人舱里的气体与外界空气相同,其中氧气的体积分数约为%;
(3)深海潜航中可观察海底的"热液"与"冷泉"现象。前者是海水渗入地下,被熔岩加热后重返海底的活动。该海水中的丰富矿物地重返地表时遭遇冷水后沉积,沉积的主要原因是:。后者的形成原因之一是海底天然气的溢出,天然气的主要成分是甲烷,完全燃烧生成二氧化碳和水,写出该反应的化学方程式:。
某矿石由
、
、
和
组成,用它制备氢氧化镁的流程示意图如图所示:
(1)溶液
中共含有种阳离子;
(2)在溶液
中加入熟石灰调节溶液的pH,可以使溶液中的阳离子转化为沉淀。该实验条件下,使金属阳离子沉淀的相关
数据见下表。为保证产品纯度、减少产品损失,并便于操作,溶液
的
可允许的范围为;
| 氢氧化物 |
|
|
|
| 开始沉淀的 | |||
| 完全沉淀的 |
(3)溶液
中一定含有的溶质为(填化学式);
(4)写出溶液
中加入熟石灰,生成产品的化学方程式:。
某同学利用以下药品:长、宽和厚度均相同的锌片、铁片和铜片,稀硫酸、硫酸亚铁溶液、硫酸铜溶液、硫酸锌溶液、锌粉,验证锌、铁、铜的金属活动性顺序。
(1)实验前,用砂纸打磨金属片的目的是:;
(2)根据实验目的,该同学设计了实验Ⅰ、Ⅱ两中合理的方案,如图所示:
若X、Y是两种不同的试剂,则X、Y中溶质的化学式依次为、;
(3)该同学将硫酸亚铁溶液和硫酸铜溶液混合在一起,溶液呈现为青色。
A.向混合液中加入过量锌粉,搅拌,溶液颜色的变化应为:青色变浅至色,最终变为无色。
B.向混合液中插入锌片,待其浸没部分表面完全变色后,溶液仍为青色,取下锌片表面附着的粉末,以检验其组成为铁和铜。粉末中存在铁的原因:
①反应生成了铁,写出该反应的化学方程式:;
②;
(4)如图所示,该同学用导线将锌片和铜片连接起来,接入电流表,然后把它们一起插入硫酸铜溶液中,该实验的现象为:①电流表;②铜片表面。