在2KMnO4+16HCl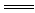 2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化产物是( )
2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化产物是( )
| A.KCl | B.MnCl2 | C.H2O | D.Cl2 |
在2FeBr2+3Cl2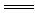 2FeCl3+2Br2的反应中,被氧化的元素是( )
2FeCl3+2Br2的反应中,被氧化的元素是( )
| A.Fe | B.Br | C.Fe和Br | D.Cl |
在氧化还原反应中,下列叙述正确的是( )
| A.物质失电子的反应为氧化反应 |
| B.物质在变化中失去了电子,此物质是氧化剂 |
| C.发生电子转移的反应即是氧化还原反应 |
| D.发生化合价升降的反应不一定是氧化还原反应 |
下列反应不一定是氧化还原反应的是( )
| A.化合反应 | B.分解反应 | C.复分解反应 | D.置换反应 |
带静电的有机玻璃棒靠近下列液体的细流,细流会发生偏转的是( )
| A.苯 | B.二硫化碳 | C.溴水 | D.四氯化碳 |