一包粉末可能含有K+、Fe3+、Al3+、Cl-、SO42-、CO32-中的若干种,现进行以下实验:
(1)取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
(2)向(1)所得溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后在滤液中加入稀硝酸酸化,然后滴入AgNO3溶液,有白色沉淀生成;
(3)取(2)中的有色沉淀加入足量的稀盐酸后,沉淀全部溶解;
(4)重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
(5)向(4)所得的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤。往得到的沉淀中加入过量的NaOH溶液,沉淀减少。
根据上述实验,这包粉末中一定不含有的离子是 ,肯定含有的离子是 ,不能确定是否含有的离子是 ,可通过 (填实验方法)来进一步确定该离子。
pH=12的氢氧化钠溶液稀释100倍后,pH=
向体积为10 L的固定密闭容器中通入3 mol X气体,在一定温度下发生如下反应:
2X(g)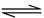 Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5min后反应达到平衡Ⅰ,此时测得容器内的压强为起始时的1.2倍,则且Y表示的反应速率为mol/(L·min);
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内反应速率分别为:甲: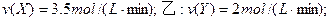 丙:
丙: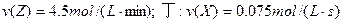 。若其它条件下同,温度不同,则温度由高到低的顺序是(填序号);
。若其它条件下同,温度不同,则温度由高到低的顺序是(填序号);
(3)若向Ⅰ的平衡体系中充入氮气,则平衡(填“向左”或“向右”或“不”)移动;若将Ⅰ的平衡体系中部分混合气体移走,则平衡(填“向左”或“向右”或“不”)移动;
(4)若在相同条件下向Ⅰ的平衡体系中再充入0.5 mol X气体,则原平衡Ⅰ中X的转化率与重新平衡后X的转化率相比较(选填字母)。
| A.无法确定 | B.前者一定大于后者 |
| C.前者一定等于后者 | D.前者一定小于后者 |
(5)若保持温度不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时各气体体积分数与Ⅰ平衡相同,且起始时维持化学反应向逆反应方向进行。则c的取值范围应该为。
Ⅰ.现有四种有机化合物: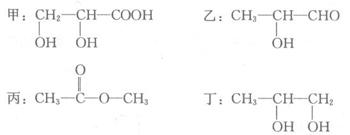
试回答:
(1)甲、乙、丁都含有的官能团名称是;
(2)1 mol甲、乙、丁分别与足量Na反应,生成H2最多的是(填编号,下同);
(3)互为同分异构体的是;
(4)等物质的量的甲、乙、丁充分燃烧,消耗氧最少的是;
(5)丁与醋酸在催化下发生取代反应生成的酯有种。
Ⅱ.白乳胶是一种在日常生活中使用广泛的有机物。某校化学兴趣小组拟用下列合成路线合成该物质: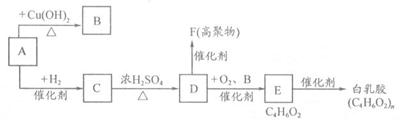
试回答:
(1)A的结构简式为;
(2)写化学方程式:
A→B;
D→E。
A、B、C、D、E、X、Y为中学常见的七种物质,它们有如下转化关系(部分产物与反应条件略去):
(1)若A为金属单质,B为氢气,X为盐酸,Y为强碱溶。则A物质的名称是;D与Y反应的离子方程式为;
(2)若A、C为同主族元素组成的单质,通常状况下,A为气体,C为液体,Y为金属单质。则A→C的反应类型是;将X通入A的溶液中,可观察到的现象是;将X通入A的溶液中,可观察到的现象是;D→E的化学反应方程式为。
常温下,浓度均为0.1 mol/L的四种溶液:
①Na2CO3溶液 NaHCO3溶液③盐酸④氨水
试回答下列问题:
(1)上述溶液中有水解反应发生的是(填编号,下同),溶液中溶质存在电离平衡的是;
(2)比较①、②溶液,PH值较大的是;
(3)在溶液④中加入少量NH4Cl固体,此时 的值将(填“变小”,“变大”或“不变”);
的值将(填“变小”,“变大”或“不变”);
(4)用溶液③滴定V mL溶液④,其滴定曲线如右图所示:
①试分析在滴定过程中,滴定曲线上a、b、c、d四点:
水的电离程度最大的是点,理由是;
;
②a点溶液中离子浓度大小关系是;
③取少量c点溶液于试管,再滴加0.1 mol/L NaOH溶液至中性。此时溶液中除H+、OH-外,离子浓度大小关系是。