A、B、C、D、E均为短周期主族元素,且原子序数依次递增。A、E同主族,B、D同周期且B和D最外层电子数之和为10;D为自然界含量最多的元素;A与D可形成A2D、A2D2共价化合物。请回答:
(1)C的气态氢化物的电子式为___ ___,其水溶液显 性。
(2)B、C、D气态氢化物稳定性由强到弱的顺序是_____ ___________(用化学式表示)。
(3)与E同周期的元素中,金属性最弱的金属元素名称是 ,原子结构示意图为: ,其最高价氧化物对应的水化物与E的最高价氧化物对应的水化物的溶液反应的离子方程式为 。
(4)E、C两元素的最高价氧化物对应水化物的稀溶液各0.1mol,恰好完全反应,放出5.73kJ的热量,写出此反应的热化学方程式: 。
有A、B、C、D、E五种易溶于水的强电解质,它们由如下离子组成(各种离子不重复)。
| 阳离子 |
H+、NH4+、Mg2+、Ba2+、Al3+ |
| 阴离子 |
OH-、Cl-、HCO3-、NO3-、SO42- |
 已知:①0.1 mol/L A溶液中C(H+)>0.1mol/L ;
已知:①0.1 mol/L A溶液中C(H+)>0.1mol/L ;
②将B溶液分别与其它四种溶液混合,均有白色沉淀生成;
③C溶液 白色沉淀。请回答下列问题:
白色沉淀。请回答下列问题:
(1)写出下列物质的化学式:A______________、B______________。
(2)写出“C溶液 白色沉淀”有关反应的离子方程式___________________。
白色沉淀”有关反应的离子方程式___________________。
(3)D、E两种物质中必有一种是_______________,写出将少量该物质的溶液滴加到B溶液中反应的离子方程式_______________________________________________________。
(4)请你设计实验确定C及另一种未知物各是什么物质。(只许在A~E中选择检验试剂)
| 实验步骤 |
预期现象和结论 |
| 取适量C的溶液于试管中, ① 。 |
预期现象和结论1: ②; 预期现象和结论2: ③; |
锰、铝、铁、钠的单质及其化合物在工业生产中有着广泛应用。请回答下列问题:
(1)工业上可用铝与软锰矿(主要成分为MnO2)反应来冶炼锰。
①用铝与软锰矿冶炼锰的原理是(用化学方程式来表示)。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是。
(2)将一定量的铁粉在氯气中燃烧后所得固体溶于水可得到溶液X。取少量X溶液两份,一份加入KSCN溶液时,溶液显红色;另一份中加入黄色铁氰化钾 (K3[Fe(CN)6])溶液后能发生复分解反应生成蓝色沉淀。已知:K3[Fe(CN) 6]的电离方程式为K3[Fe(CN)6]= 3K++[Fe(CN) 6]3-。请分析:
①用化学方程式表示产生两种金属阳离子的原因。
②蓝色沉淀是由铁氰化钾与低价态阳离子反应的结果,试写出该反应的离子方程式。
(3)将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入HCl气体6.72L(标准状况),若忽略反应过程中溶液的体积变化。
请完成下列问题:
①反应过程中共得到的气体的体积为(标准状况);
②最终是否有沉淀产生?(填“是”或“否”),若有沉淀产生,其质量为。 (若不存在,则不必回答第(2)问)
(1)室温下,向Na2S的水溶液中加入等体积等浓度的盐酸,反应后所得的溶液中,除氢离子之外的离子浓度由小到大的顺序为:
(2)常温下将0.2mol/LHCl溶液与0.2mol/LMOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,求出混合溶液中下列算式的结果(填具体数字):
c(Cl-)-c(M+)= mol/L; c(H+)-c(MOH)= mol/L。
(3)已知:室温下H2CO3的电离常数K1=4.2×10-7,K2=5.6×10-11,则pH为8.0的NaHCO3溶液中C(CO32-):C(HCO3-)=。
(4)工业上可以通过电解NO制备 NH4NO3,其工作原理如下图所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是_______, 阴极的电极反应______________。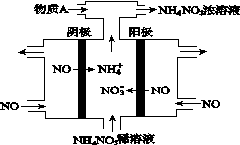
尿素 [CO(NH2)2 ]是首个由无机物人工合成的有机物。
(1)工业上尿素由CO2和NH3,在一定条件下合成,其反应方程式为。
(2)当氨碳比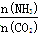 =4,CO2的转化率随时间的变化关系如图所示.
=4,CO2的转化率随时间的变化关系如图所示.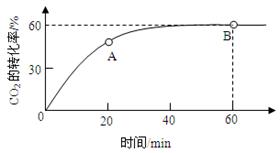
①A点的逆反应速率v逆(CO2)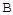 点的正反应
点的正反应
速率为v正(CO2)(填“大于”、“小于”或“等于”)
②NH3的平衡转化率为。
(3)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图
①电源的负极为(填“A”或“B”).
②阳极室中发生的化学反应用方程式表示,依次为、。
③电解结束后,阴极室溶液的pH与电解前相比将;若两极共收集到气体13.44L(标准状况),则除去的尿素为g(忽略气体的溶解).
向某密闭容器中加入0.3mol A、0.08mol C和一定量的B三种气体,一定条件下发生反应,各物质浓度随时间变化如下左图所示。右图为t2时刻后改变容器中条件,平衡体系中速率随时间变化的情况,且四个阶段都各改变一种条件,所用条件均不同。已知t3~t4阶段为使用催化剂。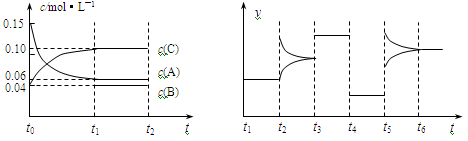
(1)若t1 = 15s,则t0~t1阶段以C浓度变化表示的反应速率为v(C) = 。
(2)若t2~t3阶段,C的体积分数变小,此阶段没有平衡前v(正) v(逆) (填“>”、“=”、“<”)。
(3)t4~t5阶段改变的条件为,B的起始物质的量为。
(4)t1达到平衡后,若保持容器温度和体积不变,再向容器中加入0.08 mol A,0.2mol C则平衡。(向左移动,向右移动,不移动)