铬酸铅俗称铬黄,不溶于水。广泛用于涂料、油墨、漆布、塑料和文教用品等工业。实验室模拟工业上用铬污泥(含有Cr2O3、Fe2O3、Al2O3、SiO2等)制备铬黄的工艺流程如下: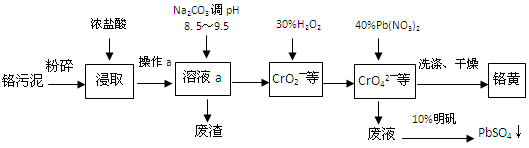
(1)将铬污泥粉碎的目的是 。操作a的名称为 。
(2)废渣的主要成分是Al(OH)3和Fe(OH)3。已知25℃时,Al(OH)3的Ksp=1.3×10—33,则该温度下反应Al3+ + 3H2O  Al(OH)3 +3H+的平衡常数为 。
Al(OH)3 +3H+的平衡常数为 。
(3)写出加入30%H2O2过程中发生的离子反应方程式: 。
(4)加入Pb(NO3)2沉淀CrO42—时,检验沉淀是否完全的方法是 。
(5)在废液中加入10%明矾溶液发生反应的化学方程式为 。
有机物A是一种纯净的无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实验步骤 |
解释或实验结论 |
| (1)称取A物质 18.0 g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为:________ |
(2)A的核磁共振氢谱如下图: |
(2)A中含有______种氢原子 |
| (3)另取A 18.0 g与足量的NaHCO3粉末反应,生成0.2 mol CO2,若与足量钠反应则生成0.2 mol H2。 |
(3)写出A中所含官能团的名称: |
| (4)将此18.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者依次增重10.8 g和26.4 g。 |
(4)A的分子式为: |
| (5)综上所述A的结构简式____________________。 |
(1)中国古代四大发明之一——黑火药,它的爆炸反应为
2KNO3+3C+S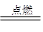 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
①在生成物中,A的晶体类型为,含极性共价键的分子的中心原子轨道杂化类型为。
②除S外,上列元素的电负性从大到小依次为。
(2)①已知CN—与N2结构相似,推算HCN分子中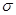 键与
键与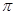 键数目之比为。
键数目之比为。
②原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为,Q2+的未成对电子数是。
③在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++xR—H→Rx[CrCln(H2O)6-n]+xH+
交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。 将含0.0015 mol [CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1 NaOH溶液25.00 ml,该配离子的化学式为。
(14分) A、B、C、D、E是原子序数依次增大的短周期主族元素,A、D在周期表中的相对位置如下表;A元素最低负化合价的绝对值与其原子最外层电子数相等;C是地壳中含量最多的金属元素。
| A |
||||
| D |
(1)A与氢元素组成的化合物分子有6个原子,其结构简式为_____________,写出该化合物在常温下使溴水褪色的化学方程式______________________________,该化合物还是一种重要的化工原料,写出其加聚生成高分子的化学方程式:____________________________。
(2)B元素的最高氧化物对应的水化物与它的氢化物反应得到离子化合物,则B元素的单质分子空间构型为___________,写出该单质的一种等电子体:_________________。
(3)C的离子结构示意图为____________,元素E在周期表中的位置是_________________。
(14分)A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大.B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族.B、C、D的最高价氧化物的水化物均能互相反应生成盐和水.A和E可形成离子化合物,其晶胞结构如下图所示: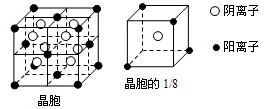
(1)A、C、D、E四种元素依次是____ ____ ____ ____ (用元素符号表示)。
(2)上述四种元素ABCD中第一电离能最小的是________电负性最大的是________其原子半径由小到大的顺序为________________(均用元素符号表示)。
(3)A和D的氢化物中,前者沸点较高,原因是________________________________。
(4)A和E的化合物晶体中,每个阳离子的周围与它最近且等距离的阳离子共有个________。
(12分)下列物质:①H2②HF ③H2O2 ④KF ⑤NH4Cl ⑥C2H2⑦N2H4+⑧BF3⑨H2O ⑩N2(填序号)
(1)只含非极性键的是___________________
(2)只含极性键的极性分子是_____________
(3)既有极性键又有非极性键的是_________
(4)只有σ键的是_______________________
(5)既有σ键又有π键的是_______________
(6)含有配位键的是_____________________