雄黄(AS4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为 。
(2)上述反应中的氧化剂是 ,反应产生的气体可用 吸收。
(3) As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3—=2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成2mol H3AsO4,则反应中转移电子的物质的量为 。若将该反应设计成一原电池,则NO2应该在 (填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量 (选填编号)。
a.小于0.5 mol b.等于0.5 mol c.大于0.5mol d.无法确定
组成生命细胞的11种宏量元素(约占人体总质量的99.97%),全部位于周期表的前20号。其中组成人体蛋白质、脂肪、碳水化合物和核酸的主要有6种元素。
(1)这六种元素中除H、C、O、P、S外,应该还有____(写元素符号),它的原子最外层共有种不同运动状态的电子;与它同周期,且单质熔点最高的元素在周期表中的位置。
(2)糖类是人体获得能量的来源之一。已知1mol葡萄糖在人体内完全氧化为二氧化碳和水,放出2804 kJ的热量,该反应的热化学方程式____。
(3)CO2是一种温室气体,它的电子式为,将其转变其他化工原料,必须破坏的化学键属于____.(填“极性”或“非极性”)键。
(4)元素周期表中元素的性质存在递变规律,下列关系正确的是____(填序号)。
a.离子半径:S2-> Na+'>O2->H+ b.与水反应的剧烈程度:K>Na>Mg>Ca
c.熔点:CO2>SiO2>Na2O>SO3 d.还原性:PH3>H2S>HCl>HF
(5)下表为部分非金属元素与氢形成共价键的键长与键能数据:
根据表中数据,归纳共价键键能与键长的关系。
(15分)某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色:J分子内有两个互为对位的取代基。在一定条件下有如下的转化关系:(无机物略去)
 (1)①A物质的名称为:______。(2分) ②X E+K的反应类型是______。(2分)
(1)①A物质的名称为:______。(2分) ②X E+K的反应类型是______。(2分)
(2)G、F中所含的含氧官能团的名称分别为___________、___________。(各1分)
(3)E与H反应的化学方程式是________________________________;(2分)
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物I,
B→I的化学方程式________________________________________;(2分)
(5)已知J有多种同分异构体,符合下列性质的J的同分异构体共有_____种。(3分)
①与FeCl3溶液作用显紫色; ②与新制Cu(OH)2悬浊液作用产生红色沉淀;
③苯环上的一卤代物有2种。写出其中一种一氯代物的结构简式____________(2分)
请回答
(1)若甲、乙、X均是化合物,Y是单质,则Y可能是。(填化学式,下同)
(2)若酸性X>Y,且甲过量,Y是白色浑浊,则Y是乙是(各1分)
(3)若甲、乙是金属单质,X为固体,则反应的化学方程式是
(4)甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体。X、Y是化合物。X溶液呈淡绿色,Y的溶液能使KSCN溶液变红。
①将Y的饱和溶液滴入沸水中,继续加热可得红褐色液体丙,证明丙的操作、现象及结论
是(3分)
②单质甲、乙和Y溶液中的阳离子氧化性由强到弱的顺序为:(用化学式表示)
③当X与甲1:1充分反应的离子方程式:(2分)
[化学——-选修5:有机化学基础]有机物A为芳香烃类化合物,质谱分析表明其相对分子质量为104,分子中含有碳碳双键,F为有香味的有机化合物,G是一种能制成塑料的高分子化合物,其相关反应如下图所示: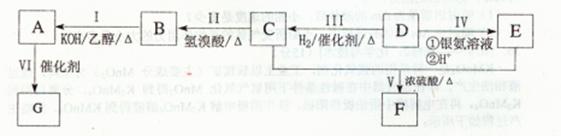
(1)D中所含官能团为_______。
(2)II的反应类型为 _______,G的结构简式为_______。
(3)写出下列反应的化学方程式: I:_______;V;_______。
(4)若A分子中的一个H原子在一定条件下被Cl原子取代,互为顺反异构体,它们的结构简式为_______。
(5)E有多种同分异构体,其中含有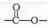 结构,且苯环上含有两个取代基的有____种,其中在核磁共振氢谱中只出现4种峰的所有物质的结构简式为:_______
结构,且苯环上含有两个取代基的有____种,其中在核磁共振氢谱中只出现4种峰的所有物质的结构简式为:_______
[化学——选修3:物质结构与性质]W、Q、R、X、Y、Z六种元素的原子序数逐渐增大。已知W原子Is轨道上只有一个电子,Q、X原子p轨道的电子数分别为2和4,Z的原子序数为29,除Z外均为短周期主族元素,Y原子的价电子排布为msnMpn。请回答下列问题:
(1)Q和W能形成一种化合物的相对分子质量为28,则该化合物的中心原子采取的杂化轨道类型是_______,该分子中含有____个 键。
键。
(2)Z原子的核外电子排布式为_______;向Z的硫酸盐中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体,该晶体中Z的离子与NH3之间的化学键为_______。
(3)这六种元素中,电负性最大与最小的两种非金属元素形成的晶体属于____晶体;Q、R、X三种元素的第一电离能数值由小到大的顺序为_______(用元素符号回答)。
(4)元素X的阴离子Xn-中所有电子正好充满K和L电子层,CnX晶体的最小结构单元如图所示。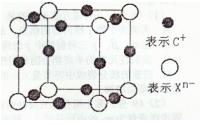
该晶体中阳离子和阴离子个数比为____,晶体中每个Xn-被_______ 个等距离的C+离子包围。