氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是 ;
;
(2)基态B原子的电子排布图为 ; BN中B元素的化合价为 ;
(3)在BF3分子中,F—B—F的键角是 ,B原子的杂化轨道类型为 ;
(4)已知: BF3 + NaF(过量)= NaBF4;化合物NaBF4含有的化学键类型为 ;BF4-中F—B—F的键角是 ,B原子的杂化轨道类型为 ,BF4-的立体构型为 ;
(5)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的相互作用为 ,层间作用力为 。含1 mol BN的六方氮化硼晶体中含B-N的个数为 NA。
某不饱和有机物结构为CH3─CH═CH─COOH,该化合物不可能发生的反应是
| A.加成反应 | B.酯化反应 | C.水解反应 | D.与碳酸氢钠溶液反应 |
下列物质不能和氢氧化钠溶液反应的是
| A.氨基乙酸 | B.乙醇 | C.油酸甘油酯 | D.醋酸铵 |
某试管中盛有碘的苯溶液,加入少量的乙酸乙酯,充分振荡,静置片刻后
| A.整个溶液变蓝色 | B.整个溶液显紫红色 |
| C.上层无色,下层紫红色 | D.上层紫红色,下层无色 |
下图为番茄电池,下列说法正确的是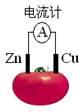
| A.一段时间后,锌片质量会变小 | B.铜电极附近会出现蓝色 |
| C.电子由铜通过导线流向锌 | D.锌电极是该电池的正极 |
据报道,氢燃料电池公交汽车已经驶上北京街头。下列说法正确的是
| A.电解水制取氢气是理想而经济的制氢方法 |
| B.发展氢燃料电池汽车不需要安全高效的储氢技术 |
| C.氢燃料电池把氢气和氧气燃烧放出的热能转化为电能 |
| D.氢燃料电池汽车的使用可以有效减少城市空气污染 |