某温度下,H2 (g) + CO2 (g)  H2O(g) + CO(g) (ΔH>0)的平衡常数
H2O(g) + CO(g) (ΔH>0)的平衡常数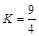 ,该温度下在甲、乙、丙、丁四个恒容的密闭容器中投入原料的起始浓度如下表:
,该温度下在甲、乙、丙、丁四个恒容的密闭容器中投入原料的起始浓度如下表:
| 起始浓度(mol/L) |
甲 |
乙 |
丙 |
丁 |
| c(H2) |
0.01 |
0.02 |
0.02 |
0.005 |
| c(CO2) |
0.01 |
0.01 |
0.02 |
0.005 |
| c(H2O) |
0 |
0 |
0 |
0.005 |
| c(CO) |
0 |
0 |
0 |
0.005 |
下列判断有错的是
A.平衡时,乙中CO2的转化率>60%
B.平衡时,四容器中甲的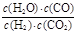 值最小
值最小
C.起始时丁向正反应方向进行
D.反应开始时,丙中反应速率最快
分别往含有下列离子的溶液中通入氯气,离子浓度不会减少的是 ( )
| A.H+ | B.HC03一 | C.OH- | D.Ag+ |
在强酸性溶液中能大量共存的无色透明离子组是()
| A.Mg2+ Na+ Cl- SO42- | B. K+ Na+ NO3- CO32- |
| C. K+ Na十 Cl- Cu2+ | D. Na十 Ba2+ OH- SO42- |
下列中和反应对应的离子方程式能以“H+ + OH—= H2O”表示的是()
| A.醋酸和氢氧化钠溶液反应 | B.氨水和盐酸反应 |
| C.氢氧化钡和稀硫酸反应 | D.澄清石灰水和硝酸反应 |
下列离子方程式中,书写不正确的是()
| A.氯化钠溶液中加入硝酸银溶液:Ag+ + Cl- = AgCl↓ |
| B.把金属钠放入水中:Na + 2H2O =" Na+" +2OH- + H2 |
| C.将氯水加入碘化钾溶液中:Cl2 + 2I- ="" 2Cl- + I2 |
| D.盐酸滴在石灰石上:CaCO3 + 2H+ =" Ca2+" + CO2↑ + H2O |
下列叙述正确的是()
| A.将73gHCl溶于水中配成1L溶液,所得溶液物质的量浓度是2mol/L |
| B.水的摩尔质量是18g |
| C.在标准状况下,1mol任何物质的体积都约为22.4L |
| D.标准状况下,1.8L H2O和1.8L NH3 所含分子个数相同 |