“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题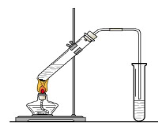
(1)在大试管中按一定比例将乙醇、乙酸混合后充分加热,在右边小试管中未收集到有香味的液体(气密性良好),原因可能是: 。
(2)右边小试管中应加入的试剂是: ;其作用是 。
(3)下列描述能说明乙醇与乙酸的酯化反应已达到该反应的限度的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
(4)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图: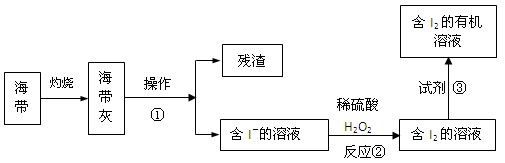
操作①的名称是 ;反应②的离子方程式是 ,下述物质中可做试剂③的是 。
| A.乙醇 | B.苯 | C.乙酸 | D.四氯化碳 |
实验室制配0.40mol/L的NaCl溶液80mL,有以下仪器:
①烧杯②100 mL量筒③100 mL容量瓶④500 mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)⑦药匙
(1)配制该溶液应选用___________mL容量瓶;
(2)向容量瓶中加入蒸馏水,到液面________________________时,改用___________加蒸馏水至液面最低点与刻度线相切,最后_________(填所选字母:A.左右旋转 B.上下颠倒)摇匀。
(3)取80ml配制好的溶液,加水稀释到200ml,这浓度变为。
(4)配制一定物质的量浓度的溶液,造成浓度偏高的操作是
A.定容时,滴加蒸馏水超过刻度线
B.未洗涤烧杯和玻璃棒
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时,眼睛仰视刻度线
(1)下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
|
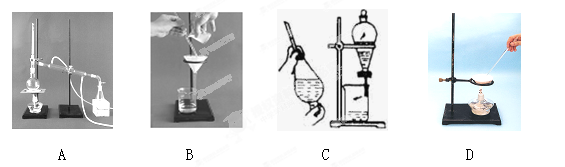
实验题(本题共10分)
(1)现有三组混合液:①乙酸乙酯和乙酸钠溶液②乙醇和水⑧溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是()
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
(2)某化学课外小组用海带为原料制取了少量碘水.现用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液.其实验操作可分解为如下几步:
(A)把50毫升碘水和15毫升CCl4加入分液漏斗中,并盖好玻璃塞;(B)把盛有溶液的分液漏斗放在铁架台的铁圈中;(C)倒置漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;(D)检验分液漏斗活塞和上口的玻璃塞是否漏液;(E)旋开活塞,用烧怀接收溶液;(G)静置,分层(F)将分液漏斗上口倒出上层水溶液;(H)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;就此实验。完成下列填空:
①正确操作步骤的顺序是:(用上述各操的编号字母填写)
___→___→___→→→____→→
②上述(E)步骤的操作中应注意;上述(H)步骤操作的目的是。
③能选用CCl4从碘水中萃取碘的原因是。
④下列物质,不能作为从溴水中萃取溴的溶剂的是。
A.热裂汽油 B.苯 C.酒精 D.正庚烷
(共17分)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加,该过程的现象为:。
(2)步骤②加入过量H2O2的目的:。
(3)步骤③中反应的离子方程式:。
(4)步骤④中一系列处理的操作步骤:过滤、、灼烧、、称量。
(5)若实验无损耗,则每片补血剂含铁元素的质量g。
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+→5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管外,还需。
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是。
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
③滴定到终点时的现象描述为 ________________
(共14分)某中学化学实验小组为了证明和比较SO2和氯水的漂白性,设计了如下装置:
(1)实验室常用装置E制各Cl2,写出该反应的离子方程式__________________________指出该反应中浓盐酸所表现出的性质
(2)反应开始后,发现B、D两个容器中的品红溶液都褪色,停止通气后,给B、D两个容器加热,两个容器中的现象分别为:BD
(3)装置C的作用是
(4)该实验小组的甲、乙两位同学利用上述两发生装置按下图装置继续进行实验:
通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅。试根据该实验装置和两名同学的实验结果回答问题。
①试分析甲同学实验过程中,品红溶液不褪色的原因是:。(用离子方程式进行说明)
②你认为乙同学是怎样做到让品红溶液变得越来越浅的?