下列物质的转化或分离是用哪种方法实现的?
| A.溶解 | B.裂解 | C.分馏 | D.裂化 |
E.干馏 F.蒸馏 G.电解 H.过滤
I.萃取 J.渗析 K.盐析
请将所选方法的字母代号填在横线上(每一项只填写一种最主要的方法,用字母填空)。
(1)把煤转化为焦炉气、煤焦油和焦炭等
(2)除去粗盐溶液中的泥沙
(3)从海水得到的无水MgCl2中提取金属镁
(4)从碘水中提取碘
(5)获得短链不饱和烃,如乙烯、丙烯、丁二烯等
(6)除去淀粉溶液中所含的食盐
I. 今有H2、Cl2混合气100 mL(标况),其中一种气体的体积为45mL。光照使两种气体发生反应后恢复到标况,气体体积为mL。为了说明反应后气体中H2或Cl2有剩余,使气体通过10 mL水,并使剩余气体干燥后恢复到标况,
(1)若仍剩余___mL,证明有___剩余,理由是_____;
(2)若溶液有___性质,证明有___剩余,理由是________________________。
II.一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧化性强弱的微型装置(如图所示)。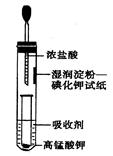
(1)下列溶液能吸收Cl2的是________。
| A.饱和食盐水 | B.Na2SO4溶液 |
| C.NaOH溶液 | D.浓硫酸 |
(2)能说明Cl2的氧化性强于I2的实验现象是_______________________。
(3)实验室制取氯气的离子方程式__________________________。
现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。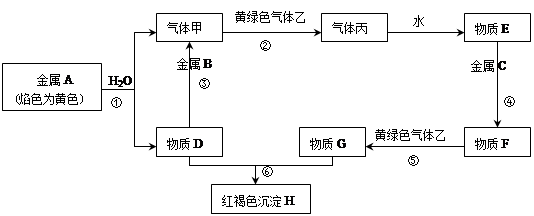
请回答下列问题:
(1)写出下列物质的化学式:B、丙、乙。
(2)写出下列反应的化学方程式:
反应①;
反应⑤;
反应⑥。
用18mol/L的硫酸配制100 mL 1.0 mol/L的硫酸,若实验仪器有:A、100mL量筒;B、托盘天平;C、玻璃棒;D、50 mL容量瓶;E、10 mL量筒;F、胶头滴管;G、50 mL烧杯;H、100 mL容量瓶。
(1)实验时选用的仪器是________;(填仪器序号)
(2)在容量瓶的使用方法中,下列操作不正确的是()
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心的倒入容量瓶中,加入蒸馏水到接近刻度线2—3cm处,再用滴管滴加蒸馏水到刻度线
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线2—3cm处,再用滴管滴加蒸馏水到刻度线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动几次
Ⅰ:某些化学反应可表示为:A+B→C+D+H2O,请回答下列问题:
(1)若A、C、D均是铁的化合物,B是稀硫酸,则A与B反应的化学方程式为
(2)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,该反应离子方程式为。
(3)若A为淡黄色固体,C为无色的气体,则该反应的离子方程式为。
Ⅱ:某些化学反应可表示为:A+NaOH+H2O→C+D。请回答下列问题:
(1)若A为金属单质,C为非金属单质,写出符合要求的离子方程式_____________________
(2)若A为非金属单质,C为非金属单质,写出符合要求的化学反应方程式
(一)实验室用Na2CO3·10H2O配制500ml 0.10mol·L-1的Na2CO3溶液,填空并请回答下列问题:
(1)根据实验要求填表:
| 应量取Na2CO3·10H2O的质量/g |
应选用容量瓶的规格/mL |
除容量瓶外还需要的其它玻璃仪器 |
(2)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次);
A.用适量水洗涤烧杯2—3次,洗涤液均注入容量瓶中,振荡。
B.用托盘天平准确称量所需Na2CO3·10H2O的质量,倒入烧杯中,再加入适量水,用玻璃棒慢慢搅动,使其溶解(需要时可加热)。
C.将已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(3)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?若没有进行A操作;若加蒸馏水时不慎超过了刻度;若定容时俯视刻度线。
(二)喷泉实验是一种常见的自然现象,其产生原因是存在压强差。试根据下图,回答下列问题:
(1)在图A的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是()。
A.HCl和H2OB.Cl2和NaOH溶液
C.HCl和汽油D.CO2和NaOH溶液
(2)在图B的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是()
A.Cu与稀盐酸B.NaHCO3与NaOH溶液
C.CaCO3与稀硫酸 D.NH4HCO3与稀盐酸
(3)在图B的锥形瓶外放一水槽,锥形瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质不可能是()。
A.浓硫酸 B.生石灰 C.硝酸铵 D.烧碱
(4)比较图A和图B两套装置,以产生喷泉的原理来分析,图A是_______上部烧瓶内压强;城市中常见的人造喷泉及火山爆发的原理与上述________(填图A或图B)装置的原理相似。