常温,向浓度为0.1mol/L,体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。根据图像回答下列问题: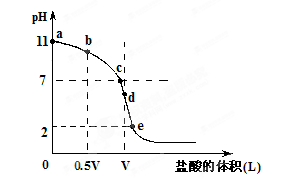
(1)氨水的电离方程式为 ,该温度时氨水的电离平衡常数K= 。
(2)比较b、c、d三点时的溶液中,水电离的c(OH-)大小顺序为 。
(3)滴定时,由b点到c点的过程中,下列各选项中数值保持不变的有 。
(4)根据以上滴定曲线判断下列说法正确的是(溶液中N元素只存在NH4+和NH3.H2O两种形式) 。
| A.点b所示溶液中:c(NH4+)+c(H+)=c(NH3.H2O)+c(OH-) |
| B.点c所示溶液中:c(Cl-)=c(NH3.H2O)+c(NH4+) |
| C.点d所示溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.滴定中可能有:c(NH3.H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
(5)滴定过程中所用盐酸的pH= ,d点之后若继续加入盐酸至图像中的e点(此时不考虑NH4+水解的影响),则e点对应的横坐标为 。
请同学们根据官能团的不同对下列有机物进行分类。
(1)芳香烃:;(2)卤代烃:;
(3)醇:;(4)酚:;
(5)醛:;(6)酮:;
(7)羧酸:;(8)酯:。
利用反应Zn +2FeCl3=ZnCl2+2FeCl2,设计一个原电池,在下面画出实验装置图:
并指出正极为,电极反应式;
负极为电极反应式为。
(1)AgNO3的水溶液呈(填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示):;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以(填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈性 ,原因是(用离子方程式表示):
__________________________________________________ 。
物质的量浓度均为0.1mol/L的下列溶液:①KNO3 、②Na2CO3 、③NaHCO3 、④NaHSO4 、⑤CH3COOH、⑥NaOH、⑦Ba(OH)2 、⑧NH4Cl,pH由大到小的顺序为:
(填数字代号)
下列盐溶液中能发生水解的用离子方程式表示,不能发生水解的请写上“不发生水解”字样并说明溶液的酸碱性:
1)CH3COOK ,溶液呈性;
2)K2SO4,溶液呈性;
3)CuCl2,溶液呈性。