(16分)A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示(部分产物略去):
(1)若A是能使湿润的红色石蕊试纸变蓝的气体,C、D均为空气的主要成分,E是一种有毒气体.
①C的电子式为_______________.
②写出反应Ⅱ的化学方程式______________________.
(2)若A是淡黄色化合物,常温下D是无色气体,C中含有的阴、阳离子均为10电子粒子.
①C中所含化学键的类型是____________.
②写出反应Ⅲ的离子方程式______________________.
(3)将(2)中一定量的气体D通入2 L C的溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量关系如图所示(忽略气体的溶解和HCl的挥发).
①O点溶液中所含溶质的化学式为_____________,a点溶液中各离子浓度由大到小的关系是_______________.
②标准状况下,通入气体D的体积为_____L,C溶液的物质的量浓度为_____mol·L-1.
尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应分为如下两步:
第1步:2NH3(l)+CO2(g) H2NCOONH4(氨基甲酸铵) (l)△H1=" —330.0" kJ·mol-1
H2NCOONH4(氨基甲酸铵) (l)△H1=" —330.0" kJ·mol-1
第2步:H2NCOONH4(l) H2O(l)+H2NCONH2(l)△H2="+226.3" kJ·mol-1
H2O(l)+H2NCONH2(l)△H2="+226.3" kJ·mol-1
(1)写出工业合成尿素的热化学方程式:
(2)下列措施中有利于提高尿素的产率的是___________。
| A.采用高温 | B.采用高压 | C.添加高效催化剂 | D.定时分离尿素 |
(3)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图所示: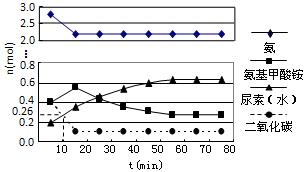
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第步反应决定。
②反应进行到10 min时测得CO2的物质的量如上图所示,则用CO2表示的第一步反应的速率v(CO2)=。
(4)工业上合成氨常与尿素生产联合进行以提高经济效益,合成氨的热化学方程式如下:
N2(g) + 3H2(g)  2NH3(g)△H = —92.4 kJ/mol
2NH3(g)△H = —92.4 kJ/mol
请在答题卡的坐标图中,画出反应过程中体系的能量变化图(进行必要的标注)。
(5)有一工业投产前小实验:在一定温度和压强下,将6 molH2和2 molN2在2L密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的体积分数约为11.1%(即1/9),此时H2的转化率是多少?(写出计算过程,计算结果保留3位有效数字。)
龙胆酸甲酯是制取抗心律失常药物——氟卡尼的中间体。
I、已知龙胆酸甲酯结构如图所示。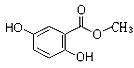
(1)龙胆酸甲酯的分子式为,它的含氧官能团名称为。
(2)下列有关龙胆酸甲酯的描述,不正确的是(填字母)。
| A.不能发生消去反应 | B.难溶于水 |
| C.能与溴水反应 | D.能与碳酸钠溶液反应产生二氧化碳 |
(3)龙胆酸甲酯与足量氢氧化钠溶液反应的化学方程式是
。(不用写反应条件)
II、已知X及其他几种有机物存在如下转化关系,且测得转化过程中的C4H8为纯净物: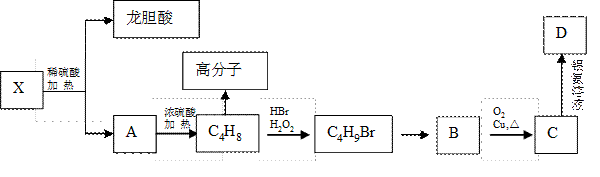
回答以下问题:
(4)写出满足下列条件的龙胆酸的一种同分异构体的结构简式
①能发生银镜反应;②能使FeCl3溶液显色;③酯类。
(5)写出B生成C的化学方程式,它的反应类型是
反应。
在密闭容器中进行:
反应① Fe(s)+CO2(g) FeO(s)+CO(g)△H1=" a" kJ·mol-1
FeO(s)+CO(g)△H1=" a" kJ·mol-1
反应② 2CO(g)+O2(g) 2CO2(g)△H2=" b" kJ·mol-1
2CO2(g)△H2=" b" kJ·mol-1
反应③ 2Fe(s)+O2(g) 2FeO(s)△H3
2FeO(s)△H3
(1)△H3=(用含a、b的代数式表示)
(2)反应①的化学平衡常数表达式K=,已知500℃时反应①的平衡常数K=1.0,在此温度下2L密闭容器中进行反应①,Fe和CO2的起始量均为2.0mol,达到平衡时CO2的转化率为,CO的平衡浓度为
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则a0(填“>”、“<”或“=”)。为了加快化学反应速率且使体系中CO的物质的量增加,其它条件不变时,可以采取的措施有(填序号)。
| A.缩小反应器体积 | B.再通入CO2 |
| C.升高温度 | D.使用合适的催化剂 |
(4)下列图像符合反应①的是(填序号)(图中ν是速率、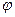 为混合物中CO含量,T为温度)。
为混合物中CO含量,T为温度)。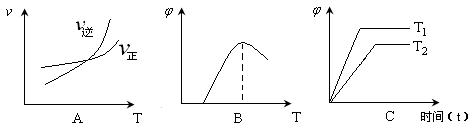
A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。它们的结构简式如下所示: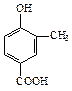
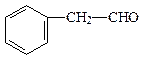
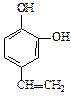
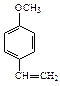
A BCD
回答下列问题:
(1)A中的含氧官能团名称是
(2)B与足量氢气充分反应的产物的结构简式为
(3)化合物C的分子式为 ,1 mol该物质完全燃烧需消耗 mol O2
(4)D发生聚合反应的产物的结构简式为
(5)A能与乙醇发生反应生成一种有特殊香味的物质,请写出该反应的方程式:
(6)关于上述四种物质的说法中正确的是
A.都能与Na反应放出H2
B.C、D均能使溴的四氯化碳溶液褪色
C.A和C均能与NaHCO3溶液反应放出CO2
D.1molC最多能与4molBr2发生反应
(相对原子质量:Na 23 O 16 H 1)
(1)配制物质的量浓度为0.2 mol/L的NaOH溶液500 mL,填空并请回答下列问题:
| 应称量NaOH的质量/g |
已给仪器 |
除已给仪器外还需要的其他仪器 |
| 烧杯、药匙、 托盘天平 |
(2)下列操作对配制的NaOH溶液浓度有偏高影响的是_______
| A.称量NaOH固体时,露置在空气的时间过长 |
| B.选用的容量瓶内有少量的蒸馏水 |
| C.在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中 |
| D.在定容时仰视容量瓶刻度线 |
(3)向0.1 mol/L的AlCl3溶液中加入过量的0.2 mol/L的NaOH溶液,则发生反应的离子方程式为
(4)将配制好的0.2 mol/L的NaOH溶液逐滴加入到0.1 mol/L的Ca(HCO3)2溶液中,则发生反应的离子方程式为