工业品MnCl2溶液中含有Cu2+、Pb2+等离子,加入过量难溶电解质MnS,可使Cu2+、Pb2+等离子形成沉淀,以制取纯净MnCl2。由此可推知MnS
| A.具有吸附性 | B.溶解度小于CuS、PbS |
| C.溶解度与CuS、PbS相同 | D.溶解度大于CuS、PbS |
设NA为阿伏伽德罗常数的数值,下列说法正确的是
| A.标准状况下,22.4L盐酸含有NA个HCl分子 |
| B.1L0.1mol·L-1的氨水中含有0.1NA个NH4+ |
| C.1molNa被完全氧化生成Na2O2,失去2NA个电子 |
| D.常温常压下,8gO2含有4NA个电子 |
传统的自来水消毒常采用漂白粉等强氧化剂,但其产生的有机氯对人体有一定的危害。一种新型的消毒剂——高铁酸盐(如Na2FeO4或K2FeO4)能有效地杀灭水中的细菌和病毒,同时其产物在水中经过变化后能除去水中的微细悬浮物。在以上变化过程中不可能涉及的变化有
| A.电离 | B.水解 | C.置换反应 | D.氧化还原反应 |
下列变化属于氧化还原反应的是
| A.馒头在咀嚼过程中产生甜味 |
| B.三氯化铁溶液长期放置产生红褐色固体 |
| C.蛋白质溶液中加入饱和硫酸铵溶液,析出沉淀 |
| D.植物油长期放置发生“酸败产生刺激性气味” |
下列物质分类正确的是
| A.SO2、SiO2、CO均为酸性氧化物 |
| B.稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C.烧碱、冰醋酸、四氯化碳均为电解质 |
| D.福尔马林、水玻璃、氨水均为混合物 |
按图甲装置进行实验,实验结果如图乙所示。乙中横坐标x表示电路中通过电子的物质的量,纵坐标y表示反应物或生成物的物质的量,下列叙述不正确的是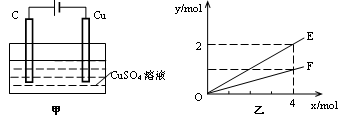
| A.E表示反应生成铜的物质的量 | B.E表示反应消耗水的物质的量 |
| C.F表示反应生成氧气的物质的量 | D.F表示反应生成硫酸的物质的量 |