26下图为实验室常用的实验装置,回答问题:
(2)若用A、C装置组合制取氧气,收集氧气完毕时,应先 (填“熄灭酒精灯”或“从水中取出导气管”),写出A装置中发生反应的化学方程式 。
(3)写出用B、E装置组合制取某气体的化学反应方程式 。
(4)硫化氢(H2S)是有毒气体,能溶于水形成氢硫酸(氢硫酸是硫化氢的水溶液,其化学性质与盐酸相似)。实验室通常用块状固体硫化亚铁(FeS)和稀硫酸混合,在常温下发生反应制得H2S。某同学用右图F、G、H装置组合来收集H2S气体。
①F用于收集H2S,说明其密度比空气 (填“大”或“小”)。
②G装置的作用是 ,H装置的作用是 。
为检测某化工厂排放的废液中是否含有SO42-,同学们设计了如下方案,并进行了实验。
| 方案 |
步骤 |
现象 |
结论 |
| Ⅰ |
①取样品,滴加BaCl2溶液 ②对步骤①反应后的混合物进行过滤,在滤渣中滴加稀盐酸 |
①有白色沉淀产生 ②无明显现象 |
废液中含有SO42﹣ |
| Ⅱ |
①取样品,滴加过量_____________ ②在步骤①的溶液中滴加BaCl2溶液 |
①无明显现象 ②有白色沉淀产生 |
废液中含有SO42- |
| Ⅲ |
①取样品,滴加Ba(NO3)2溶液 ②对步骤①产生的混合物进行过滤,在滤渣中滴加稀硝酸 |
①有白色沉淀产生 ②无明显现象 |
废液中含有SO42- |
(1)方案Ⅱ的实验结论如果正确,步骤①中滴加的物质是 。21世纪教育网
(2)方案Ⅰ和Ⅲ中,结论不成立的方案是 ,理由是 。
(3)方案Ⅲ的滤渣中,滴加稀硝酸是为了排除 的干扰。
在学习过程中,可以判断反应发生的方法有多种。
(1)向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
| 烧杯中溶液的pH |
1.1 |
1.2 |
1.4 |
1.6 |
2.0 |
7.0 |
11.0 |
12.2 |
当加入氢氧化钠溶液的体积为mL时,稀盐酸和氢氧化钠溶液恰好完全反应。
(2)在图的实验中,当观察到的现象是 就可证明NaOH与HCl发生了反应。
(3)不使用指示剂或pH试纸等方法,也可证明反应发生。向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该合理的物质是 。
小佳在实验室中发现一种黑色粉末和一瓶标签破损的无色溶液(如图所示),她取少量黑色粉末与溶液混合,发现立即产生了大量无色的气泡。
已知:稀硫酸(H2SO4)+Fe→硫酸亚铁(FeSO4)+H2
(1)对这两种物质是什么她进行了大胆猜想。小佳的猜想可能是:
猜想①;
猜想②稀硫酸(H2SO4)和铁粉;理由是。
(2)请你帮助小佳同学完成实验,以证明猜想①是正确的。
| 实 验 步 骤 |
实 验 记 录 |
实 验 结 论 |
| (i) 取少量黑色粉末于试管中,滴加少量无色溶液 (ii) |
(i) 有气泡产生 (ii) |
产生的气体是,发生化学反应的符号表达式为 原猜想①成立。 |
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热在相同温度下,比较两组实验产生O2的快慢。
Ⅱ中x的值应为________。
②乙探究了影响双氧水分解速度的某种因素。实验数据记录如下:
| 双氧水的质量 |
双氧水的浓度 |
MnO2的质量 |
相同时间内产生O2体积 |
|
| Ⅰ |
50.0g |
1% |
0.1g |
9 mL |
| Ⅱ |
50.0g |
2% |
0.1g |
16 mL |
| Ⅲ |
50.0g |
4% |
0.1g |
31 mL |
本实验中,测量O2体积的装置是________(填编号)。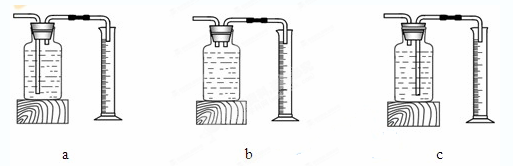
实验结论:在相同条件下,_______________,双氧水分解得越快。
丙用下图装置进行实验,通过比较____________也能达到实验目的。
注射器是一种普通的医疗器械,但它在化学实验中发挥着越来越大的作用。某化学兴趣小组为了测定空气中氧气的含量,进行了如下探究活动:
[选择药品 ] 小光小组认为,选择的药品的理由是①既要能消耗氧气,又不会与空气中的其他成分反应,②。他们应该选择()
| A.蜡烛 | B.硫粉 | C.红磷 | D.铁丝 |
[查阅资料] 白磷的着火点是40℃,红磷的着火点是240℃,两种物质的 燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,能与空气中的水蒸气反应,生成有毒的偏磷酸(HPO3)。
[设计实验]小明小组设计了如图的装置进行探究活动。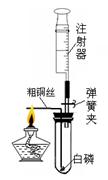
[步骤与现象]
①测量试管的容积为50mL;
②检查装置的气密性良好;
③装药品,将注射器活塞调整到合适位置,连接好仪器;
④用弹簧夹夹紧胶皮管,加热粗铜丝,观察现象;
⑤燃烧结束,试管冷却到室温后打开弹簧夹,观察注射器活塞的移动情况。
[反思与交流]
(1)实验中利用了铜丝的__________性。
(2)兴趣小组同学测量试管容积的方法可能是________________ 。
(3)步骤③中注射器吸水使活塞至少应调到____________mL处(填整数)。
(4)步骤④中观察到试管中的现象有________________________;
(5)小华同学认为步骤⑤在保证活塞自由移动的前提下,观察活塞位置时,最好将试管和注射器整体横放,小华同学的理由是。