A、B、C、D都是初中化学中的常见物质,具有如图所示的转化关系(反应条件、有些反应物或产物已略去):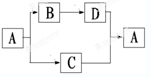
(1)若A是一种白色难溶于水的钙盐,由三种元素组成,C 是大气循环循环中的一种重要物质.则B的化学式是 ,C和D反应生成A的化学方程式是 。
(2)若A是无色液体,D是一种黑色固体.则C的化学式是 ,由B生成D的化学方程式为 。
(3)若A是碳酸氢钠,且已知碳酸氢钠受热可分解为碳酸钠、二氧化碳和水.写出过量的气体C与D溶液反应生成A的化学方程式 。
氮元素的单质和常见的化合物在工、农业生产中用途广泛。
(1)工业上利用分离空气的方法得到氮气。空气各主要成分的沸点如下:
| N2 |
O2 |
Ar |
CO2 |
| —196°C |
—183°C |
—186°C |
—78°C |
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是 。
(2)雷雨时空气中的N2转化为NO,生成物NO是 色的气体, (填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应。NO2与水反应的化学方程式为 。
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气。
①制取氨气的化学方程为 ;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为 g。
(4)已知:4NH3+6NO 5N2+6 H2O 。化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。
5N2+6 H2O 。化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。
|

某同学想利用原电池反应探究Zn和Cu的金属活动性顺序。请你帮他选择适宜的材料和试剂设计一个原电池,并完成下列实验报告:
实验目的:探究Zn和Cu的金属活动性顺序
(1)电极材料:正极:;负极:;电解质溶液为H2SO4溶液。
(2)写出正极反应式:。
(3)请画出该原电池装置图:
实验现象:负极不断溶解,正极上气泡产生
实验结论:。
(14分)
I、人们常利用化学反应中的能量变化为人类服务。
(1)煤是一种重要的燃料,在点燃条件下燃烧,放出大量的热。其在燃烧过程中能量的变化与如图所示中的(填字母代号)最相符。 (2)将一定量的碳酸钠晶体与硝酸铵晶体密封于一塑料袋中,用线绳绑住塑料袋中间部分,使两种晶体隔开,做成“冰袋”。使用时将线绳解下,用手使袋内两种固体粉末充分混合,便立即产生低温,这种“冰袋”可用于短时间保鲜食物。则碳酸钠与硝酸铵的总能量_____________(填“高于”或“低于”)反应后生成产物的总能量。
(2)将一定量的碳酸钠晶体与硝酸铵晶体密封于一塑料袋中,用线绳绑住塑料袋中间部分,使两种晶体隔开,做成“冰袋”。使用时将线绳解下,用手使袋内两种固体粉末充分混合,便立即产生低温,这种“冰袋”可用于短时间保鲜食物。则碳酸钠与硝酸铵的总能量_____________(填“高于”或“低于”)反应后生成产物的总能量。
(3)化学反应中的能量变化不仅仅表现为热能的变化,有时还可以表现为其它形式的能量变化。比如,停电时,人们一般点蜡烛来照明,这主要是将化学能转化为;人们普遍使用的干电池,是将化学能转化为。
II、某同学在超市看到一种电池外壳的纸层包装印有如获至宝图的文字,请根据要求回答问题。
(1)该电池的种类是__ ___(填序号)。
①干电池②蓄电池③燃料电池
(2)该电池含有的金属元素中毒性最大的是_ __ __(写元素符号)。
(3)该电池的使用和性能,说法正确的是__ ___
A.该电池可应用于闹钟、收音机、照相机等
B.该电池可充电后反复使用
C.该电池使用后不能投入火中,应埋入地下以防污染环境
(10分)已知A、B、C、D、E是短周期的5种元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出B、D元素的名称:B,D。
(2)画出C元素的离子结构示意图。
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式
(4)A、B、C三种元素形成的化合物所含的化学键类型为。
(5)B、C、D三种元素的离子半径由大到小的排列顺序为(用离子符号表示)。
W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素;Z元素的最高正化合价为+6。Y和W的最外层电子数相等。Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍。由此可知:
(1)写出元素符号:W为,X为,Y为,Z为;
(2)Y2Z是由键组成的物质,其电子式为;
(3)由Y、X、W组成的物质中有键和键,形成的是化合物;
(4)用电子式表示Z与钙形成化合物的过程。