1994年度诺贝尔化学奖授予为研究臭氧做出贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3的分子结构如图,呈V型,两个O----O键的夹角为116.5o。三个原子以一个O原子为中心,另外两个O原子分别构成一个共价键;中间O原子提供2个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键------三个O原子均等地享有这4个电子。请回答: 
(1)臭氧与氧气互为____________________,
(2)下列分子中与O3分子的结构最相似的是_____(填选项字母);
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
(3)分子中某原子有一对或几对没有跟其他原子共用的价电子叫孤对电子,那
么O3分子有 对孤对电子。
(4)O3分子是否为极性分子 。(填是或否)
(5)O3具有强氧化性,它能氧化PbS为PbSO4而O2不能,试配平:
_____ PbS +_____ O3 ="===_____" PbSO4 + _____ O2
生成1mol O2的转移电子物质的量为__________ mol。
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
请回答下列问题:
(1)流程甲通入过量CO2后生成沉淀F的离子反应方程式为______________________________________。
(2流程乙加入烧碱溶解SiO2的化学反应方程式____________________。
(3)验证滤液B含Fe3+,可取少量滤液并加入________(填试剂名称)。
(4)滤液E、K中溶质的主要成分是________(填化学式),写出该溶质的一种用途____________________。
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的滤液B,加入一定量的烧碱至达到沉淀溶解平衡,测得pH=12,则此温度下残留在溶液中的c(Mg2+)=________________。
相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。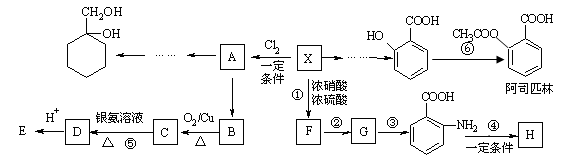
已知:
Ⅰ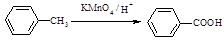
Ⅱ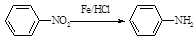 (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与本题所给信息回答下列问题:
(1)H的结构简式是______________;(2)反应②的类型是______________;
(3)反应⑤的化学方程式是____________________________________________;
反应⑥的化学方程式是____________________________________________;
(4)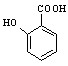 有多种同分异构体,其中符合下列条件的共有__________种
有多种同分异构体,其中符合下列条件的共有__________种
①能发生银镜反应但不能水解
②每摩尔同分异构体最多消耗2mol NaOH
③苯环上一氯代物只有两种
一定温度下2升的恒容容器甲中,加入2moL碳和2moLCO2发生如下反应: C(s)+CO2(g)  2CO(g) △H>0,测得容器中CO2的物质的量随时间t的变化关系如图所示。
2CO(g) △H>0,测得容器中CO2的物质的量随时间t的变化关系如图所示。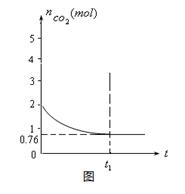
(1)该反应的ΔS0(填“>”、“<”或“=”)。在(填“较高”或“较低”)温度下有利于该反应自发进行。
(2)列式并计算上述温度下此反应的平衡常数K。
(结果保留一位小数)
(3)向上述平衡体系中再通入CO2,则CO2的转化率(填增大、减小、不变、无法确定)。
(4)相同温度下,2升的恒容容器乙中加入4moL碳和4moLCO2,达到平衡。请在图中画出乙容器中CO2的物质的量随时间t变化关系的预期结果示意图。(注明平衡时CO2的物质的量)
(5)相同温度下,2升的恒容容器丙中加入4moL碳、4moLCO2和4moLCO。开始反应时
V(正)V(逆)(填>、<、﹦)。
短周期的五种元素A、B、C、D、E,原子序数依次增大。A、B、C三种元素电子层数之和是5。A、B两元素原子最外层电子数之和等于C元素原子最外层电子数;B元素原子最外电子层上的电子数是它的电子层数的2倍, A与D可以形成原子个数比分别为1:1和2:1的两种液态化合物;E单质用于净化水质。
请回答:
(1)写出D在元素周期表中的位置,E的原子结构示意图是_____。
下列可以验证C与D两元素原子得电子能力强弱的实验事实是__________(填写编号);
A.比较这两种元素的气态氢化物的沸点
B.比较只有这两种元素所形成的化合物中的化合价
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(2)由A、B两种元素组成的最简单的化合物,写出其电子式。
(3)均由A、B、C、D四种元素组成的甲、乙两种化合物,都既可以与盐酸反应又可以与NaOH溶液反应,甲为无机盐,其化学式为,乙为天然高分子化合物的水解产物,且是同类物质中相对分子质量最小的,其结构简式为。
(4)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:
①将化合物CA3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程的总的离子方程式________________________。
②上述反应生成的两种碱继续作用,得到Fe3O4
(5)已知下表数据:
| 物质 |
Fe(OH)2 |
Fe(OH)3 |
| Ksp/25℃ |
2.0×10-16 |
4.0×10-36 |
若使混合液中FeSO4、Fe2(SO4)3的浓度均为2.0mol·L-1,则混合液中c(OH-)不得大于mol·L-1。
NaNO2俗称“工业盐”,其外观与食盐相似,易误食而中毒,可通过化学实验加以鉴别。如向NaNO2的酸性溶液中加入KI固体,析出的碘可以使淀粉溶液变蓝色,据此检验NO2—。
请回答下列问题:
(1)写出上述反应的离子方程式。
(2)日常生活中若需鉴别工业盐和食盐,现有碘化钾淀粉试纸,则还需选用的生活中常见物质的名称为。
(3)某工厂废切削液中含有2%—5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2转化为不引起污染的N2,该物质是,
a.NaCl b.H2O2 c.NH4Cl d.浓H2SO4
所发生反应的离子方程式为:。