某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0 g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下:
| 所加盐酸的次数 |
第一次 |
第二次 |
第三次 |
第四次 |
| 烧杯及所盛物质总质量/g |
181.2 |
204.4 |
228.6 |
253.6 |
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线。(不要求写出计算过程,只画出曲线即可)
(10南通)25.我国采用食盐中加入碘酸钾的方法防止缺碘引起的疾病。 (1)在人体中,碘是属于 ▲(选填“常量”或“微量”)元素。
(1)在人体中,碘是属于 ▲(选填“常量”或“微量”)元素。 (2)碘酸钾(KIO3)中钾、碘、氧三种元素质量比为 ▲;它受热易分解,烹饪时,添
(2)碘酸钾(KIO3)中钾、碘、氧三种元素质量比为 ▲;它受热易分解,烹饪时,添
加加碘食盐应注意 ▲。
(3)我国规定加碘食盐含碘量为20mg/kg~50mg/kg。为测定某加碘食盐是否为合格产品。在酸性条件下用足量KI溶液将其中KIO3全部转化成I2。反应方程式为:KIO3+5KI+6HCl=6KCl+3I2+3H2O。称取1000g某品牌加碘盐样品进行测定,经测定反应获得的I2的质量为152.4 mg,试通过计算说明该加碘食盐是否为合格产品(计算过程写在答题纸上)。
(10常州26).16g Fe2O3与184g稀H2SO4恰好完全反应,求所得Fe2(SO4)3溶液的溶质质量分数。
(10盐城2.)取黄铜屑(铜锌合金)32.5g,放入盛有180g稀硫酸(足量)的容器中充分反应,生成氢气0.4 g。试计算(请写出解题过程):
(1)该黄铜屑中铜的质量。
(2)反应的溶液蒸发掉多少克水后可变成20%的硫酸锌溶液?
(10四川甘孜23) “节能减排”已经引起当今社会普遍关注。化石燃料燃烧会产生大量的CO2,大气中CO2含量过高会导致温室效应等环境问题。
(1)计算1000g CH4完全燃烧产生CO2的质量m;
(2)从下表数据分析,与煤相比,用天然气做燃料的优点是。
| 1000g物质完全燃烧产生CO2的质量 |
1000g物质完全燃烧放出的热量 |
|
| CH4 |
m |
5.6×104KJkJ |
| C |
3.67×103g |
3.2×104KJg |
(10江苏泰州27)“钾泻盐”的化学式为MgSO4·KCl·xH2O,是一种制取钾肥的重要原料,它溶于水得到KCl与MgSO4的混合溶液。某化学活动小组为了测定“钾泻盐”中KCl的质量分数,设计了如下两种实验方案:
方案一: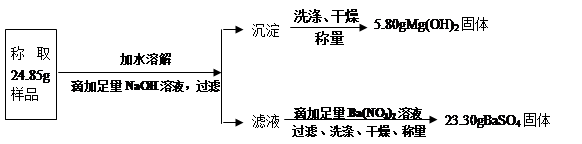
方案二: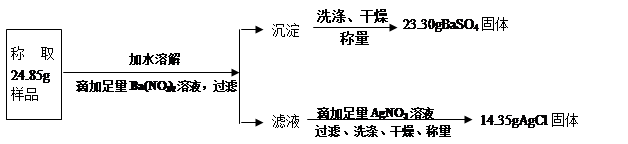
试回答下列问题:
(1)你认为方案 ▲比较合理,理由是 ▲。
(2)请选择上述方案中的数据,计算24.85g钾泻盐样品中MgSO4的质量。(写出计算过程) ▲ 。
(3)请选择上述方案中的数据,计算24.85g钾泻盐样品中KCl的质量分数。(写出计算过程) ▲。