工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)  CH30H(g)
CH30H(g)
(1)不同温度下的平衡转化率与压强的关系如图所示。
①该反应△H O,△S 0(填“>”或“<”),则该反 自发进行(填“一定能”、“一定不能”、“不一定”)
②实际生产条件控制在250℃、l,3×l04kPa左右,选择此压强的理由是 。
(2)某温度下,将2molCO和6mOlH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)="O.l" mol·L -1。
①该反应的平衡常数K= :
②在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有
关说法正确的是 (填序号)。
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH30H)增大
③若保持同一反应温度将起始物质改为a mol CO、b mol H2、c mol CH30H,欲使平衡混合物中各组成与原平衡相同,则a、b应满足的关系为 ,且欲使开始时该反应向逆反应方向进行,c的取值范围是 。
在恒温恒容的密闭容器中,通入x mol N2和y mol H2发生反应N2 + 3H2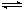 2NH3,达平衡后,测得反应放出的热量为18.4 kJ,混合气体总的物质的量为3.6 mol,容器内的压强变为原来的90%。又知N2和H2的转化率相同。
2NH3,达平衡后,测得反应放出的热量为18.4 kJ,混合气体总的物质的量为3.6 mol,容器内的压强变为原来的90%。又知N2和H2的转化率相同。
⑴通过计算说明起始充入N2和H2的物质的量分别为:x =,y = 。
。
⑵若起始加入N2、H2和NH3的物质的量分别为a mol、b mol、c mol,达平衡时各物质的含量与上 述平衡完全相同。
述平衡完全相同。
①若c=2,在相同的条件下达平衡时,该反应吸收的热量为kJ。
②若维持反应向正反应方向进行,则起始时c的取值范围为。
叠氮化合物应用广泛,如NaN3可用于汽车安全气囊,Hg(N3)2可作雷管的起爆剂,工业上制备NaN3的化学反应为:
I.N2H4(联氨) + HNO2→ HN3(叠氮酸) + H2O (未配平);
+ HNO2→ HN3(叠氮酸) + H2O (未配平);
II.HN3 + NaOH →NaN3 + H2O
⑴上述反应I中,每生成4.3g HN3时,消耗联氨的物质的量为,NaN3受撞击时迅速分解为两种单质,该反应的化学方程式为。
⑵联氨的电子式为。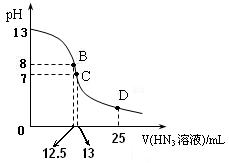
⑶上图为常温下向25mL、0.1mol/L NaOH溶液中逐滴滴加0.2mol/L的HN3溶液的过程中溶液pH的变化曲线。(溶液混合时体积的变化忽略不计)
① D点时溶液中各离子的浓度由大到小的顺序为
D点时溶液中各离子的浓度由大到小的顺序为
② B点时溶液中c  (HN3
(HN3 ) =
) =
mA、B、C是三种常见短周期元素的单质。常温下D为无色液体,E是一种常见的温室气体。其转化关系如图(反应条件和部分产物略去)。试回答: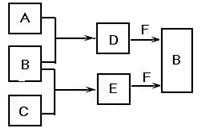
(1)单质X和B或D均能反应生成黑色固体Y,Y的化学式是。
(2)物质Z常用于对空气进行杀菌、净化和水果保鲜等。Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18。Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是。
(3)取0.3 mol F与足量D充分混合后,所得溶液中再通入0.2 mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+)。
(4)E的大量排放会引发很多环境问题。有科学家提出,用E和H2合成CH3OH和H2O,对E进行综合利用。25℃,10 1 kPa时,该反应的热化学方程式是。
1 kPa时,该反应的热化学方程式是。
(已知甲醇的燃烧热△H=-726.5 kJ/mol,氢气的燃烧热△H=-285.8 kJ/mol )
快乐是什么?精神病学专家通过实验发现:在大脑的相应部位—“奖赏 中心”,给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统。多巴胺结构如图。
中心”,给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统。多巴胺结构如图。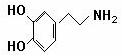
(1)多巴胺分子式:
(2)写出与多巴胺互为同分异构体且符合下列条件的物质的结构简式:
a属于1、3、5三取代苯b苯环上直接连有一个羟基和一个氨基
c分别能与钠和氢氧化钠反应,消耗钠与氢氧化钠的物质的量之比为2∶1
(3)多巴胺可由香兰素与硝基甲烷缩合,再经锌汞齐还原水解而得。合成过程表示如下: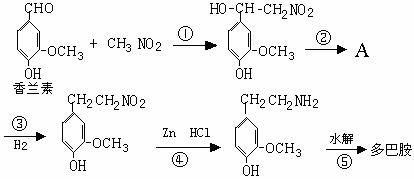
Ⅰ、写出下列反应类型:反应①,反应②
Ⅱ、写出第②、⑤ 步的化学方程式
步的化学方程式
②:⑤:
(11分) 已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属;D、H均为气体,且常温下易反应。各物质的转化关系如下图(部分反应物已略去)。请回答下列问题: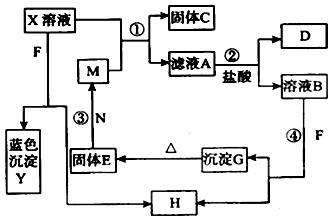
(1)F的电子式为
(2)在反应①②③④中属于置换反应的是(填序号)。
(3)反应②的离子方程式为
(4) 用石墨作电极电解50mL X溶液,观察到a电极表面有红色的固态物质生成,b电极有无色气体生成;电解一段时间后,取出a电极,洗涤、干燥、称量,电极增重1.6g。请回答下列问题:
①写出电解时的阳极反应式:。
②电解后溶液的pH为(假设电解前后溶液体积不变)。
(5)X溶液与F反应的总化学方程式为