(选做题16分)工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为:CrO42- Cr2O72-
Cr2O72-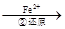 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=2,该溶液显 色。
(2)能说明第①步反应达平衡状态的是 。
A.Cr2O72-和CrO42-的浓度相同
B.2v (Cr2O72-)=" v" (CrO42-)
C.溶液的颜色不变
(3)第②步中,还原1molCr2O72-离子,需要 mol的FeSO4 7H2O。
7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在沉淀溶解平衡,请写出其沉淀溶解平衡方程式
常温下,Cr(OH)3的溶度积Ksp=[Cr3+]·[OH−]3=10−32,要使c(Cr3+)降至10−5mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(5)用Fe做电极的原因是 。
⑹在阴极附近溶液pH升高的原因是(用电极反应解释) ,溶液中同时生成的沉淀还有 。
选择合适的装置分离提纯下列物质,将装置序号填入表格:
①②③④
| 题号 |
混合物 |
方法 |
| (1) |
海水中提取饮用水 |
__________ |
| (2) |
提取碘水中的碘 |
__________ |
| (3) |
分离MnO2和NaCl固体混合物 |
溶解、 、洗涤______ |
硝基苯甲酸乙酯在OH-存在下发生水解反应:
O2NC6H4COOC2H5+OH- O2NC6H4COO-+C2H5OH
O2NC6H4COO-+C2H5OH
两种反应物的初始浓度均为0.050 mol·L-1,15 ℃时测得O2NC6H4COOC2H5的浓度c随时间变化的数据如表所示。回答下列问题:
| t/s |
0 |
120 |
180 |
240 |
330 |
530 |
600 |
700 |
800 |
| c/mol·L-1 |
0 |
0.036 |
0.030 |
0.026 |
0.022 |
0.017 |
0.016 |
0.015 |
0.015 |
(1)计算该反应在120~180 s间的平均反应速率_________;比较120~180 s与180~240 s 区间的平均反应速率的大小,前者_________后者(填>,<或=),理由是____________________。
(2)计算15 ℃时该反应的平衡常数_____________。
(3)为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可采取的措施有________。
A.加入O2NC6H4COOC2H5 B.增加OH-的浓度
C.移去产物D.加入适当的催化剂
电化学原理在化学工业中有广泛的应用.请根据如图回答问题:
(1)装置Ⅰ中的X电极的名称是 ,Y电极的电极反应式为 ,工作一段时间后,电解液的PH将 (填“增大”、“减小”、“不变”).
(2)若装置Ⅱ中a、b均为Pt电极,W为饱和食盐水(滴有几滴酚酞),实验开始后,观察到b电极周围溶液变红色,其原因是(用电极反应式表示) ,a电极上有气泡产生,该气体的电子式为 .
(3)若利用装置Ⅱ进行铜的精炼,则a电极的材料为 ,工作一段时间后装置Ⅱ电解液中c(Cu2+)将 (填“增大”、“减小”、“不变”).
(4)若装置Ⅱ中a为Ag棒,b为铜棒,W为AgNO3溶液,工作一段时间后发现铜棒增重2.1.6g,则流经电路的电子的物质的量为 .
(1)化学键的键能是指气态原子间形成1 mol化学键时释放的能量。下表列出了某些化学键的键能:
| 化学键 |
H—H |
O==O |
O—H |
| 键能(kJ·mol-1) |
436 |
x |
463 |
请回答下列问题:
①如图表示某反应的能量变化关系图,此反应为 (填 “放热”或“吸热”)反应,其中ΔH= kJ·mol-1(用含C和D的字母表示)。
②若此能量变化关系图表示反应H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则B= kJ·mol-1,x=
(2)①火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。已知:
N2H4(l)+O2(g)=N2(g)+2H2O(g),ΔH=-534 kJ·mol-1
H2O2(l)=H2O(l)+ O2(g),ΔH=-98 kJ·mol-1
O2(g),ΔH=-98 kJ·mol-1
H2O(l)=H2O(g),ΔH=+44 kJ·mol-1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式___________________。
②肼(N2H4)—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。该电池放电时,负极的电极反应式是_____________________。
标准状况下,22.4LHCl气体溶于50mL水再配成250mL溶液,求:
(1)所得盐酸的物质的量浓度为 ;
(2)若将此溶液再稀释成1L溶液,则稀释后盐酸的物质的量浓度变为 ;
(3)将(2)的溶液取出250mL与足量Zn反应可以产生的H2在标准状况下的体积为 。