化学兴趣小组对某工业废水(含有
、
)中
的含量进行测定。甲、乙两同学各提出不同的测定方法:
(1)甲同学:酸碱中和法
取60g废水于烧杯中,逐渐滴入溶质质量分数为10%的
溶液(反应的化学方程式为:
),反应过程溶液pH变化如右图,求60g废水中
的质量。

(2)乙同学:沉淀分析法
改用
溶液代替
溶液测定废水中的
的含量(反应的化学方程式为:
),你认为结果会
(4分)为定量研究长期放置氢氧化钠药品变质情况,化学兴趣小组的同学设计了如下实验,其主要实验步骤如下: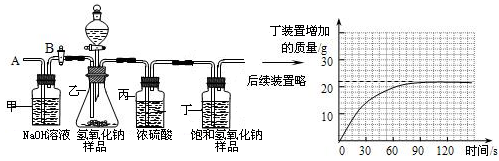
Ⅰ.按图组装仪器,将55.0g试样放入锥形瓶中,加入足量稀硫酸溶液;
Ⅱ.测量一定时间内装置丁内物质增加的质量(见下列曲线);
Ⅲ.待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓鼓入一定量的空气;
Ⅳ.再次称量装置丁内物质增加的质量;
Ⅴ.重复Ⅲ和Ⅳ的操作,直至装置丁内物质质量不变.
请根据实验数据,通过计算分析氢氧化钠变质情况(“全变质”,“部分变质”或“不变质”,要有详细的计算步骤,没有步骤不得分)
在烧杯中加入7.31g的表面氧化的锌片,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示。请回答下列问题: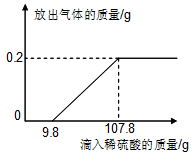
(1)产生氢气的质量是g。
(2)所滴加的稀硫酸中溶质的质量分数。
(3)锌片恰好完全反应时,溶液中溶质的质量。
实验中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。
请根据以上信息计算:
(1)生成二氧化碳的质量为克。
(2)样品中碳酸钙的质量分数为。
(3)C烧杯中溶液的溶质质量分数?
同学们做甲、乙两个中和反应实验的探究,如图所示: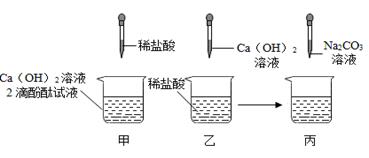
(1)甲实验恰好中和,则该溶液中的溶质是_____ (填化学式)。
(2)取乙反应后的溶液60.0g,滴加质量分数26.5%的Na2CO3溶液,如图丙,溶液pH的变化如图丁,则与CaCl2反应的碳酸钠溶液的质量为_____g;请计算该溶液中CaCl2的溶质质量分数(写出计算过程,精确到0.1%)。
(3)根据计算所得数据在图戊中画出产生沉淀的曲线。
镁条在空气中易被氧化。有一根在空气中放置一段时间的镁条样品,其质量为2.8 g,将该样品放入107.8 g稀硫酸中,两者恰好完全反应,反应过程中测得数据如下:
| 数据记录时间 |
t1 |
t2 |
t3 |
t4 |
| 剩余物质质量/g |
110.52 |
l10.46 |
l10.40 |
110.40 |
请计算(写出计算过程):
(1)反应前后减少的质量是__________g,原因是______________________________。
(2)2.8 g样品中含氧化镁的质量是多少?
(3)稀硫酸中溶质的质量分数是多少?