我国目前使用碘酸钾作为食用盐中碘强化剂。并规定,食用盐碘含量的平均水平(以碘元素计)为20 mg/kg ~ 30 mg/kg。
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式,并用单线桥标出电子转移。
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
该反应中的氧化剂是 ,氧化产物是
(2)已知:I2+2S2O32-=2 I-+S4O62-,某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取20 g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol/L的Na2S2O3溶液10.0 mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是 。
②b中反应所产生的I2的物质的量是 mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是 mg/kg。(小数点后保留一位有效数字)
某烯烃与氢气的加成产物为:CH3 CH( CH3)2该产物的系统命名的名称是
__________________;该烯烃的分子式为___________,结构简式为___ _______________.
_______________.
如图所示,实验室用NH4Cl和Ca(OH)2制取NH3。试回答下列问题:
(1)写出反应的化学方程式
(2)B处的药品是
(3)检验D处试管中NH3是否收集满,除用湿红色石蕊试纸外,还可用方法是
(4)在标准状况下,收集到224mlNH3后,将它溶于水中,恰好得到100ml氨水,则最后所得溶液的物质的量浓度为mol/L
有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。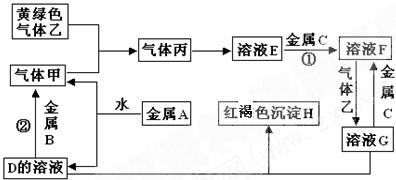

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A______________;乙;H_____________。
(2)写出下列反应的离子方程式:
反应①____________________________
(3)写出反应②的化学方程式:________________________________
现有三组混和物:①汽油和水;②碘和水;③硫酸钡和稀硫酸。分离以上各混和物的正确方法依次是:、、。
在氮的单质和常见化合物中(用N2、NH3、NH4Cl填空)
(1)常用作保护气(如填充灯泡、焊接保护等)的物质是,
(2)常用作制冷剂的物质是,
(3)能与酸反应生成盐,在常温下为气态的物质是,
(4)用作氮肥的是。