火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为 。
(2)又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为 ______________。
(2)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
_______________________________________________________________________。
按要求回答:
(1)写出电离方程式:
NaHCO3_______________________________________________________________________
H2S__________________________________________________________________________
(2)写出水解的离子方程式:
Na2CO3________________________________________________________________________
(3)用pH试纸测定0.1 mol·L-1的纯碱溶液的pH,其正确的操作是
__________________________________________________________________________________。
(4)氯化铝水溶液呈性(填酸性、中性、碱性),原因是(用化学方程式表示):_____________________ _______________________________________________ ______ 。把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是。
(5)实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以(填“促进”、“抑制”)Ag+水解。
(6)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,充分反应后溶液呈中性,则反应后溶液存在的离子有,其浓度由大到小的顺序为
,氨水的浓度a0.01 mol·L-1(填“>”、“<”或“=”)。
(7)在25℃下,向浓度均为0.20 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成沉淀(填化学式),生成该沉淀的离子方程式为;当测得溶液pH=11时,则此温度下残留在溶液中的c(Mg2+):c(Cu2+)= (已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.0×10-20)
某气态的烷烃与烯烃的混合气体9 g,其密度为同状况下H2密度的11.2倍,将混合气体通过足量的溴水,溴水增重4.2 g。
(1)混合气体的平均分子量是,根据平均分子量推测一定有的气体是。
(2)请列式计算原混合气体中另一种气体的分子式是什么?
(1)某烷烃0.1mol完全燃烧时生成11.2L CO2(标况下),则其化学式是。若其一氯代物有四种同分异构体,则该烷烃的结构简式是。
(2)将常温常压下气态的烷烃(用CnH2n+2表示)和烯烃(用CmH2m表示)按体积比5:1混合,混合气体是相同状况下等质量H2体积的1/16,则混合气体的组成为。
在下列物质中属于同一种物质的有、;互为同分异构体的有、。
(1)液氯 (2)氯气 (3)白磷 (4)红磷 (5)D (6)T
(7) 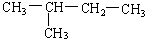 (8)
(8) 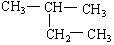 (9)新戊烷
(9)新戊烷