溴乙烷是一种难溶于水、密度约为水的密度的1.5倍、沸点为38.4℃的无色液体。实验室制取溴乙烷的反应如下:
NaBr+H2SO4(浓) NaHSO4+HBr CH3CH2OH+HBr →CH3CH2Br+H2O
NaHSO4+HBr CH3CH2OH+HBr →CH3CH2Br+H2O
已知反应物的用量:①NaBr(s) 0.3 mol,②浓硫酸36 mL(98%、密度1.84 g•cm–3),
③乙醇0.25 mol,④水25 mL,其中乙醇的密度为水的密度的4/5。
试回答:
(1)仅用如下图所示仪器安装制取和收集溴乙烷的装置,要求达到安全、损失少、不污染环境的目的,有关仪器(相关胶塞上已打合适的孔,胶管未画出。)的选择和连接顺序为 (填数字)。
(2)在实验过程中,考虑到浓硫酸性质的特殊性,试剂加入的合理顺序为________________(请填写试剂的编号);
(3)若试剂加入过快,可看到烧瓶内有红棕色气体产生,写出反应的化学方程式:
。
(4)判定有溴乙烷生成的现象是__________________________。从棕黄色的粗溴乙烷制取无色的溴乙烷,第一步可以加入蒸馏水或NaHSO3溶液,本操作中通常使用的仪器是__________。
(5)本实验的产率为60%,则可制取溴乙烷 g。
恒温恒压下,向某可变容积的密闭容器中充入3 L A和2 L B,发生如下反应:3A(g)+2B(g)  xC(g)+yD(g),达到平衡时C的体积分数为m%,若维持温度、压强不变,将0.6 L A、0.4 L B、4 L C、0.8 L D作为起始物质充入密闭容器内,达到平衡时C的体积分数仍为m%,则x=________,y=________.
xC(g)+yD(g),达到平衡时C的体积分数为m%,若维持温度、压强不变,将0.6 L A、0.4 L B、4 L C、0.8 L D作为起始物质充入密闭容器内,达到平衡时C的体积分数仍为m%,则x=________,y=________.
下图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
⑴该浓盐酸中HCl的物质的量浓度为 mol·L-1。 ⑵取用任意体积的该盐酸溶液时,下列物理量中不随所取
⑵取用任意体积的该盐酸溶液时,下列物理量中不随所取 体积的多少而变化的是。
体积的多少而变化的是。
| A.溶液中HCl的物质的量 | B.溶液的浓度 |
| C.溶液中Cl-的数目 | D.溶液的密度 |
⑶某学生欲用上述浓盐酸和蒸馏水配制500 ml 物质的量浓度为0.400 mol·L-1的稀盐酸。
①该学生需要量取 ml 上述浓盐酸进行配制。 ②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
I、用量筒量取浓盐酸时仰视观察凹液面()
II、定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水()
③该36.5%的浓盐酸,若加入等质量的水稀释后,质量分数18.25%;若加入等体积的水稀释后,质量分数18.25%(用“小于”或“等于”或“大于”来填空)
掌握仪器的名称、组装及使用方法是中学化学实验的基础,右下图为两套实验装置。

⑴写出下列仪器的名称:
①;②;④;
⑵仪器①~④中,使用时必须检查是否漏水的有。(填序号)
⑶若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有;将仪器补充完整后进行的实验操作的名称为:。现需配制250 ml 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是。
欲除去硝酸钾固体中混有的少量氯化钾杂质,某学生进行如下实验操作。回答下列问题:
⑴溶解样品。该过程所需的仪器有。
⑵向溶解后的溶液中加入适量的溶液,使氯化钾转化为沉淀。(填化学式)
⑶将混合液进行过滤,过滤装置和操作如图所示,指出图中的两处错误: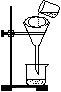
①;
②。
(1)下列每组中都有一种物质与其他物质在分类上不同,试分析每组中物质的组成规律,将这种不同于其他物质的物质找出来.
①NaCl、KCl、NaClO、BaCl2 ②浊液、溶液、胶体、水
(2)用98%的浓H2SO4(ρ=1.84 g/cm3)配制500 ml 0.5 mol/L的稀H2SO4,所需浓H2SO4的体积为________ml(小数点后保留一位有效数字),如果实验室有10 ml、20 ml、50 ml量筒,应选用ml量筒,实验中还需要用到的仪器有,若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷却至室温即转移至容量瓶进行定容________②定容时仰视刻度线
③量取好浓硫酸倒入烧杯溶解后,用水洗涤量筒2-3次,将洗涤液倒入烧杯
(3)7.8g的镁铝合金与足量的稀盐酸反应,生成氢气的体积为8.96L(标准状况),则此反应中转移电子的个数为________________,由镁和铝分别产生的氢气的体积之比为________________
(4)取100ml的Na2CO3和Na2SO4的混合溶液与过量盐酸反应,生成0.896L(标况)CO2;若向原混合溶液中加入足量的Ba(OH)2溶液,得到沉淀的质量为10.21g,试计算混合溶液中Na2CO3的物质的量浓度是___________mol/L, Na2SO4的物质的量浓度是___________mol/L。