实验室配制500 mL 0.1 mol·L-1的Na2CO3溶液,请回答下列问题。
(1)应用托盘天平称取Na2CO3·10H2O晶体 g。
(2)若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上(1 g以下用游码),天平平衡时,则实际称量的Na2CO3·10H2O晶体 g。
(3)用托盘天平和小烧杯称出Na2CO3·10H2O的质量,其正确操作顺序的标号为(操作可以重复)_______________。
| A.调整零点 |
| B.将游码移至刻度尺的零刻度处,将砝码放回砝码盒内 |
| C.将碳酸钠晶体放入小烧杯中称量 |
| D.称量空的小烧杯 |
E.记录称量结果
(4)下列操作对配得的溶液无影响的是 (填序号);会使所配溶液浓度偏大的是 (填序号)。
①在烧杯内溶解溶质,搅拌时不慎溅出少量溶液。
②容量瓶未烘干就用来配制溶液。
③定容时俯视刻度线。
④定容时仰视刻度线。
⑤定容时不小心使少量蒸馏水流出瓶外。
⑥将所配溶液从容量瓶转移到干燥、洁净的试剂瓶中时,有少量溅出。
(10分)动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
| 实验步骤 |
实验现象 |
||||
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
|
||||
| ⑤将铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
||||
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉锭。 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究 元素性质递变规律。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。仪器:① ,② ,试管,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应实验现象的编号和②的化学方程式及此实验的结论)
| 实验内容 |
① |
② |
③ |
④ |
⑤ |
⑥ |
| 实验现象(填A~F) |
① ,
② ,
此实验的结论: 。
动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
| 实验步骤 |
 实验现象 实验现象 |
||||
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
|
||||
| ⑤将铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
||||
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉锭。 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究 元素性质递变规律(填“同周期”或“同主族”)。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞 溶液等。
溶液等。
仪器:① ,② ,③ ,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式)
| 实验内容 |
① |
② |
③ |
④ |
⑤ |
⑥ |
| 实验现象(填A~F) |
① ,② ,
(4)实验结论: , 。
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如下图所示:
请回答:
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,则H2SO4 是否剩余,原因是
(2)向反应后的溶液中加入足量的CuO,过滤后将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4·XH2O)某小组同学采用加热法测定该晶体里结晶水X的值;
①冷却结晶后要获得较纯净的硫酸铜晶体采取的操作是
②在他们的每一次实验操作中至少称量次。
③加热法测定该晶体里结晶水X的值,结晶水完全失去的判断方法是 ;
④下面是三次实验数据的平均值
| 坩埚质量 |
坩埚与晶体总 质量 质量 |
加热后坩埚与固体总质量 |
| 11.7g |
22.7g |
18.6g |
根据上表数据计算出x的实测值为
(3)装置乙的作用是:;
(4)下列说法正确的是:(填序号)。
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶
b.KMnO4溶液用于尾气处理
c.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生
d.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3
(14分)某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
| 实验 |
药品 |
制取气体 |
量气管中的液体 |
| Ⅰ |
Cu、稀HNO3 |
H2O |
|
| Ⅱ |
NaOH固体、浓氨水 |
NH3 |
|
| Ⅲ |
Na2SO3固体、浓H2SO4[来 |
SO2 |
|
| Ⅳ |
镁铝合金、NaOH溶液(足量) |
H2 |
H2O |
⑴实验过程中,使用分液漏斗滴加液体的操作是。
⑵该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?(填“可行”或“不可行”),原因是.
⑶实验Ⅲ烧瓶中产生的SO2气体通入溴水溶液中,现象是.发生反应的离子方程式 是.
是.
⑷实验Ⅱ中量气管中的液体最好是____(填字母编号,下同)
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理.以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有.
⑸本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②,③视线与凹液面最低处相平.
⑹实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 |
镁铝合金度量 |
量气管第一次读数 |
量气管第二次读数 |
| ① |
1.0g |
10.0mL |
346.3mL |
| ② |
1.0g |
10.0mL |
335.0mL |
| ③ |
1.0g |
10.0mL |
345.7mL |
根据上述数据,可计算出镁铝合金中铝的质量分数为____.
高纯氧化铁(α—Fe2O3)是现代电子工业的重要材料。实验室用硫铁矿烧渣(主要成分为Fe2O3、FeO,还含有SiO2等杂质)为原料制备高纯氧化铁的步骤如下: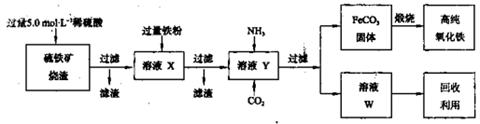
回答下列问题: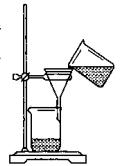 (1)上述实验所涉及的反应中,有一个反应既属于化合反应,又属于氧化还原反应。写出该反应的离子方程式:。
(1)上述实验所涉及的反应中,有一个反应既属于化合反应,又属于氧化还原反应。写出该反应的离子方程式:。
(2)实验室欲用18.4mol·L-1的浓硫酸配制100mL 5.0mol·L-1的硫酸
溶液,所用的玻璃仪器胶头滴管、量筒、烧杯、玻璃棒外,还有
(填写仪器名称)。
(3)某同学用右图所示装置进行过滤操作。
①请指出其中的错误之处:;
②过滤后,洗涤过滤器中少量沉淀的方法是。
(4)某同学用下图所示装置(尾气吸收装置未画出)实验向溶液Y中通入NH3和CO2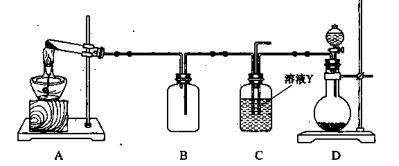
①下列为实验室制备NH3和CO2的备选药品:
a.NH4Cl b.CaCO3(块状) c.Ca(OH)2d.NaOH
e.浓氨水 f.稀盐酸 g.稀硫酸
则上述装置A处的试管中所放药品的最佳选择为和(用药品序号填空);装置D处药品的最佳选择为和(用药品序号填空)。
②下列各项制备实验中,也可利用装置D处仪器完成的是(填序号)。
| A.MnO2与浓盐酸反应制备Cl2 |
| B.Cu与浓硫酸反应生成SO2 |
| C.由KMnO4分解制O2 |
| D.乙醇与乙酸反应制备乙酸乙酯 |
E.Zn与稀硫酸反应制备H2
③写出上述装置A处的试管中所发生反应的化学方程式。
④若通入一定量的NH3和CO2后,装置C处的溶液中只含有S、N、H、O四种元素。用pH试纸测定该溶液pH的方法是;若该溶液呈中性,则溶液中的NH+4和SO2-4的物质的量浓度间的数量关系为。(离子的浓度用符号[NH+4]和[SO2-4]表示)