某结晶水合物含有两种阳离子和一种阴离子.称取两份质量均为45.3 g的该结晶水合物,分别制成溶液.向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24 L该气体(标准状况);最后白色沉淀逐渐减少并最终消失.另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g.
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是________和________,阴离子是________.
(2)该结晶水合物的化__________________________________________________.
(3)假设过程中向该溶液中加入的NaOH溶液的物质的量浓度为5 mol·L-1,请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图.
向体积为2L的密闭容器中加入2molSO2和1molO2,进行可逆反应:催化剂
2SO2+O2 2SO3反应2min后,测得O2的物质的量为0.8mol,则加热
2SO3反应2min后,测得O2的物质的量为0.8mol,则加热
(1)2min内,SO2的物质的量减少了_________ SO3的物质的量增加了____________
(2)若用O2的浓度变化来表示该反应的反应速率,则V(O2)="______________"
(3)若用SO3的浓度变化来表示该反应的反应速率,则V(SO3)=" __________"
(4)2min时SO2的转化率是____________
在下列事实中,请填写出是什么因素影响了化学反应的速率:
(1)熔化的KClO3放出气泡很慢,撒入少量MnO2很快产生气体_____________
(2)将食物放入冰箱中保鲜,不易腐烂_______________________
(3)同样大小的锌粒分别与0.1mol/LHCl和1mol/LHCl反应,反应速率不同___________
(8分)氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答下列问题:
(1)氢氧燃料电池的能量转化主要形式是____________________,在导线中电子流动方向为_________________(用a、b表示)。
(2)负极的电极反应式为____________________________________。
(3)电极表面镀铂粉的原因为______________________________ 。
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸收和放氢原理如下:
I、2Li+H2="2LiH" II、LiH+H2O=LiOH+H2↑
①反应I中的还原剂是_____________,反应中II的氧化剂是______________。
②已知用锂吸收224L(标准状况)H2,生成的LiH再与H2O作用,放出的H2用作电池燃料,若能量的转化率为80%,则导线中通过电子的物质的量为________________
如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5ml盐酸于试管中,试回答下列问题: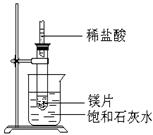
(1)实验中观察到的现象是
(2)产生该现象的原因
(3)写出有关反应的离子反应方程式
(4)有此推知,MgCl2溶等于液和H2的总能量 填 (“大于”“小于”或“”)镁片和盐酸的总能量
(共10分)已知某有机物中n(C): n(H)="1," 将W1g该有机物在足量氧气中充分燃烧,消耗标准状况下的氧气V L,产物只有CO2和H2O,且m(CO2)=w2g,m(H2O)=W3g。
(1)若通过计算来确定该有机物是否含氧,除已知的碳氢原子个数比外,还至少需上述数据中的 个,这几个数据的组合共有 种,将这些组合一一填入下列空格中。
说明:①选用V、W1、W2、W3表示,不必列出具体计算式;
②每个空格中填一种组合,有几种组合就填几种,不必填满。
(2)当W1与V之间满足 条件时,该有机物中一定没有氧原子,当W1与V之间满足 条件时,该有机物中一定含有氧原子。
(3)W1g有机物中含氧的质量为 g。(用含W1、W2的代数式表示)