现有一定量含有Na2O杂质的Na2O2试样,用图K2-6-2所示的实验装置测定Na2O2试样的纯度。(可供选用的试剂只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水)
回答下列问题:
(1)装置A中液体试剂选用____________,理由是__________________________。
(2)装置B的作用是______________________,装置E中碱石灰的作用是_____________ ____________________________。
(3)装置D中发生反应的化学方程式是:
_______ ___________________________、_______ __________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为______。
某学校化学课外活动小组的同学用粗铜(含杂质铁)按如下流程回收氧化铜晶体(CuCl2·2H2O)等相关物质。请回答下列问题:
已知Cu2+、Fe3+沉淀时的相关PH:
| 氢氧化物开始沉淀时的pH |
氢氧化物完全沉淀时的pH |
|
| Cu2+ |
4.7 |
6.7 |
| Fe3+ |
1.9 |
3.2 |
(1)为得到固体I.同学们设计下图装置:
①添加药品之前,如何检查装置A的气密性________________。
②整套装置有不足之处,要完成实验必须改进的是__________________。
③装置D的作用是__________________(用离子方程式表示)。
(2)操作Ⅱ和操作Ⅴ相同,其中所需的主要玻璃仪器有烧杯______、_______。
(3)试剂X用于调节pH以除去杂质。
①试剂X可以是_________(填字母序号)。
a.NaOHb.Cu(OH)2c.Na2CO3d.CuO
②为使CuCl2溶液中的Fe3+完全除去,溶液pH范围应保持在______,当溶液的pH=4时,c(Fe3+)=_____。[Fe(OH)3的KSP=4.0×10-38]
(4)由溶液Ⅳ欲获得氯化铜晶体(CuCl2•2H2O),应采取的措施是________。
(5)由溶液Ⅳ获得 CuCl2·2H2O晶体过程中,有同学发现溶液颜色由蓝色变为绿色进而变成黄绿色,经查阅资料发现氯化铜溶液中存在以下平衡关系: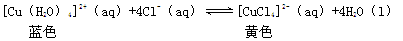
取氯化铜晶体配制成蓝绿色溶液Y,进行如下实验,其中不能证明CuCl2溶液中有上述转化关系的是___(填序号)。
a.将Y稀释,发现溶液呈蓝色
b.在Y中加入CuCl2晶体,溶液变为绿色
c.在Y中加入NaCl固体,溶液变为绿色
d.取Y进行电解,溶液颜色最终消失
甲醇是一种重要的化工原料,在生产中有着重要的应用。工业上用天然气为原料,分为两阶段制备甲醇:
(i)制备合成气:CH4(g)+H2O(g) CO(g)+3H2(g) △H1=+206.0kJ/mol
CO(g)+3H2(g) △H1=+206.0kJ/mol
(ii)合成甲醇:CO(g)+2H2(g) CH3OH(g) △H2
CH3OH(g) △H2
请回答下列问题:
(1)制备合成气:将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应(i);CH4的平衡转化率与温度、压强的关系如图1所示。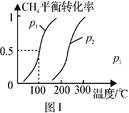
①已知100℃时达到平衡的时间为5min,则从反应开始到平衡,用氢气表示的平均反应速率为:v(H2)= 。
②图中p1 p2(填“<”、”“>”或“=”)。
③为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2,发生反应如下:
CO2(g)+H2(g) CO(g)+H2O(g),为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为 。
CO(g)+H2O(g),为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为 。
(2)合成甲醇:在Cu2O/ZnO作催化剂的条件下,向2L的密闭容器中通入1mol CO(g)和2mol H2(g),发生反应(ii),反应过程中,CH3OH的物质的量(n)与时间(t)及温度的关系如图2所示。
①反应(ii)需在 (填“高温”或“低温”)才能自发进行。
②据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量的CO2有利于维持Cu2O的量不变,
原因是 (用化学方程式表示)。
③在500℃恒压条件下,请在图2中画出反应体系中n(CH3OH)随时间t变化的总趋势图。
(3)工业上可通过甲醇羰基化法制取甲酸甲酯,其反应的热化学方程式为:
CH3OH(g)+CO(g) HCOOCH3(g)
HCOOCH3(g) 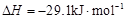 ,科研人员对该反应进行了研究,部分研究结果如下:
,科研人员对该反应进行了研究,部分研究结果如下:
①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是 (填“3.5×106Pa”、“4.0×106Pa”或“5.0×106Pa”)。
②实际工业生产中采用的温度是80℃,其理由是 。
拉氧头孢钠是一种抗生素,合成拉氧头孢钠中间体G的路线如下(部分反应物、反应条件略去):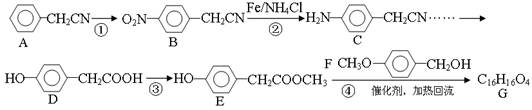
(1)A与浓硝酸发生反应①的条件是__________,反应②的反应类型是______________;
(2)F分子中官能团的名称是______________________;
(3)写出反应③的化学方程式____________________________;.
(4)D的同分异构体有多种,写出一种符合下列条件的异构体M的结构简式_______________;
Ⅰ.苯环上一氯代物只有两种;Ⅱ.遇氯化铁溶液不变色;Ⅲ.1molM最多能与2molNaOH反应;Ⅵ.核磁共振氢谱只有4个峰。
(5)已知:①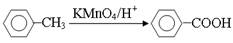 ;
;
②当苯环上已有一个“−CH3”或“−Cl”时,新引入的取代基一般在它的邻位或对位;当苯环上已有一个“−NO2”或“−COOH”时,新引入的取代基一般在它的间位。
请写出以甲苯、乙醇为原料制备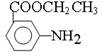 的合成路线图(无机试剂任用)。
的合成路线图(无机试剂任用)。
甲、乙组同学分别做了以下探究实验。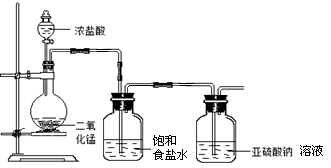
(1)甲组探究Cl2与Na2SO3溶液反应,实验装置如下。
①请指出该装置的不足之处 、 。
②Cl2与Na2SO3溶液反应的离子方程式为 。
③设计实验,简述实验步骤,证明洗气瓶中的Na2SO3已被氧化 。
乙组探究乙酸乙酯(沸点77.1℃)在不同温度、不同浓度NaOH溶液中的水解速率。
取四支大小相同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加热相同时间后,记录酯层的体积来确定水解反应的速率。
| 实验 试剂 |
试管Ⅰ(55℃) |
试管Ⅱ(55℃) |
试管Ⅲ(55℃) |
试管Ⅳ(75℃) |
| 乙酸乙酯/mL |
1 |
V1 |
V2 |
V2 |
| 1mol·L—1NaOH/mL |
V4 |
3 |
0 |
V5 |
| 蒸馏水/mL |
0 |
V6 |
5 |
2 |
④请完成上表,其中V2 = ,V4= ,V5= 。
⑤实验中,可用饱和食盐水替代蒸馏水,其优点是 ;但不能用饱和Na2CO3溶液替代蒸馏水,其原因是 。
⑥实验中,试管Ⅳ比试管Ⅱ中的酯层减少更快,其原因有:温度高速率快,还可能有 。
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。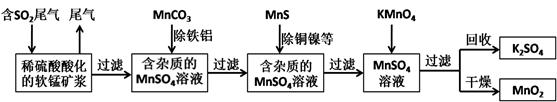
请回答下列问题:
(1)上述流程中多次涉及到过滤操作,下图表示的过滤操作中的一处错误是_______;过滤后的沉淀需要洗涤,则实验室进行沉淀洗涤的操作是 。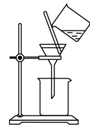
(2)用MnCO3能除去溶液中的Al3+和Fe3+,检验滤液中不存在Fe3+的实验操作是_____________。
(3)已知Ksp(CuS)=8.4×10-45,Ksp(NiS)=1.4×10-24;在除铜镍的过程中,当Ni2+恰好完全沉淀(此时溶液中c(Ni2+)=1.0×10-5mol/L),溶液中Cu2+的浓度是 mol/L。
(4)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中隋性电极作阳极,铁作阴极,请写出阴极的电极反应式 。
(5)下列各组试剂中,不能准确测定一定体积燃煤尾气中SO2含量的是__________。(填编号)
a.NaOH溶液、酚酞试液 b.稀H2SO4酸化的KMnO4溶液
c.碘水、淀粉溶液 d.氨水、酚酞试液
(6)除杂后得到的MnSO4溶液可以通过 (填操作名称)。高锰酸钾与硫酸锰反应制备MnO2的离子方程式为_____________。