写出下列元素基态原子的电子排布式:
(1) N (2)Ne
(3) S (4)Ca
(5)29Cu (6)32Ge
铁及铁的化合物应用广泛,如 FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出 FeCl3溶液腐蚀印刷电路铜板的离子方程式。。
(2)若将(1)中的反应设计成原电池,请补充右边原电池的装置图,在括号内填上正、负极的材料、电解质溶液,并写出电极反应式。正极反应
负极反应
(3)腐蚀铜 板后的混合溶液中,若 Cu2+、Fe3+和 Fe2+的浓度均为 0.10mol.L-1,请参照下表给出的数据和药品,简述除去 CuCl2溶液中 Fe3+和Fe2+的实验步骤:
板后的混合溶液中,若 Cu2+、Fe3+和 Fe2+的浓度均为 0.10mol.L-1,请参照下表给出的数据和药品,简述除去 CuCl2溶液中 Fe3+和Fe2+的实验步骤:
| 氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
| Fe3+ |
1. 9 9 |
3.2 |
| Fe2+ |
7.0 |
9.0 |
| Cu2+ |
4.7 |
6.7 |
 提供的药品:Cl2浓H2SO4 NaCl-溶液 CuO Cu 提供的药品:Cl2浓H2SO4 NaCl-溶液 CuO Cu |
实验步骤:
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的 H2还原 CuO粉末来测定 Cu的相对原子质量,同时检验氯气的氧化性。
(1)写出甲中发生反应的离子方程式
(2)为完成上述实验,正确的连接顺序为A连;B连 (填写连接的字母)。
(3)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为。
(4)若检验氯气的氧化性,则乙装置的 a瓶中溶液可以是,对应的现象为 。
(5)丙装置的 c瓶中盛放的试剂为,作用是。
(6)测定 Cu的相对原子质量:精确测量硬质玻璃管的质量为Ag,放入CuO后,精确测量硬质玻璃管和 CuO的总质量为Bg,实验完毕后精确测量硬质玻璃管和 Cu粉的总质量为cg。Cu的相对原子质量表达式(用 a、b、c表示)为。(已知氧的相对原子质量为 16)
硫铁矿烧渣(主要成分为 Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用硫铁矿烧渣制备铁红等产品的实验流程如下:
已知几种盐的溶解度随温度变化的
曲线如右图所示:
回答下列问题:
(1)酸浸、过滤后滤液中的金属阳离子是________________。
(2)煅烧 FeCO3生成产品 I的化学反应方程式为 _______。
实验室进行煅烧操作所需仪
器除了酒精喷灯、泥三角、三脚架、玻璃棒外,还有__________。
(3)产品Ⅱ的化学式为 _______________,为了获得产品Ⅱ,向 (NH4) 2SO4溶液中加入KCl溶液后,还需要进行的操作是:。
2SO4溶液中加入KCl溶液后,还需要进行的操作是:。
(4)检验产品 II中是否含有氯化物杂质的实验操作是:取少量产品Ⅱ于试管中配成溶液,。
373K时,某 1L密闭容器中加入1molPCl5发生如下可逆反应: 其中物质PCl3的物质的量变化如右图所示。
其中物质PCl3的物质的量变化如右图所示。
(1 )前 20
)前 20 s内 PCl5(g)的平均反应速率为
s内 PCl5(g)的平均反应速率为
(2)373K时该反应的平衡常数的值为
(3)若在此平衡体系中再加入 1mol的 PCl5,与原平衡比较,新平衡时 PCl5的转化率(填“增大”或“减小”,下同)。PCl5的平衡浓度。
(4)将原平衡升温至 473K,重新达平衡时(其他条件不变),PCl3的平衡浓度为 PCl5的3倍,该反应的正反应为(填“放热反应”或 “吸热反应”),为增大平衡体系中 Cl2的物质的量,下列措施正确的是(其它条件相同)
a.升高温度 b.扩大容器的体积
c.加入合适的催化剂 d.再充入 PCl3
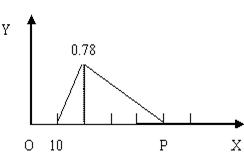
把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58g白色沉淀生成,向所得滤液(滤出0.58g沉淀),逐滴加入0.5mol/L的盐酸,加入盐酸的体积和生成沉淀的质量如图所示[图中的Y表示沉淀质量(g), x表示加入盐酸体积(mL)]
(1) 混合物中NaOH质量是____________g(2`),
MgCl2和AlCl3的物质的量之比是________(2`)
(2) P点所表示的加入盐酸的体积为________ml.(2`)