有一种蓝色晶体,它的结构特征是Fe2+和Fe3+分别占据立方体互不相邻的顶点,而CN-离子位于立方体的棱上。
(1)根据晶体结构特点,推出其化学式(用最简单整数示)________ __________________。
(2)此化学式带何种电荷?用什么样的离子(用Mn+表示)与其结合成中性的化学式?写出此电中性的化学式。
(3)指出(2)中添加离子在晶体结构中的什么位置。
(8分)化学是一门以实验为基础的学科。
(1)下列描述正确的是_____________(填写序号)。
| A.金属钠通常保存在煤油中,防止接触空气而变质 |
| B.容量瓶、分液漏斗在使用时需要检验是否漏水 |
| C.海带提取碘实验中,灼烧海带时需要用到的仪器有玻璃棒、蒸发皿、泥三角、三脚架、酒精灯 |
| D.向含有Fe2+的FeCl3溶液中通入Cl2或滴加H2O2均可以除去Fe2+ |
E.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入BaCl2溶液,产生白色沉淀,滴加稀硝酸,观察白色沉淀是否溶解
(2)实验室中常用下图仪器制取、净化和收集气体。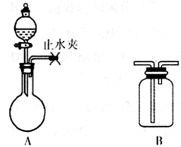
①关闭A装置中的止水夹,向分液漏斗中加入适量水,打开活塞,说明A装置气密性良好的现象是_______________________________________。
②实验室可利用A装置在加热条件下制取Cl2,写出该反应的离子方程式__________。
③若用B装置除去SO2中混有的HCl气体,B中盛放试剂的名称为_______________。
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产硫酸亚铁溶液,进而可制备绿矾(FeSO4·7H2O)、硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐)等重要试剂。生产硫酸亚铁溶液的工艺流程如下:
回答下列问题:
(1)加入少量NaHCO3,调节溶液pH的目的是__________________________。
(2)硫酸亚铁溶液在空气中久置容易变质,用离子方程式表示其变质的原因:_____。
(3)若向所得FeSO4溶液中加入少量3 moL• L-1H2SO4溶液,再加入饱和(NH4)2SO4溶液,经过蒸发浓缩、冷却结晶、过滤等一系列操作后得到硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐)。硫酸亚铁铵较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。现取0.352g Cu2S和CuS的混合物在酸性溶液中用40.00 mL0.150 mol•L-1 KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
反应后煮沸溶液,剩余的KMnO4恰好与50.00mL 0.200 mol•L-1 (NH4)2Fe(SO4)2溶液完全反应。
①配平离子方程式:MnO4-+Fe2++H+——Mn2++Fe3++H2O
②Cu2S和CuS的混合物在酸性溶液中用0.150 mol•L-1 KMnO4溶液处理后,溶液需煮沸的原因是:_______________________________________________。
③实验室配制500mL 3 moL• L-1H2SO4溶液,需要质量分数为98%,密度为1.84g• mL-1硫酸的体积为__________ mL。(保留1位小数)
④试计算混合物中CuS的质量分数(写出计算过程)。
科学家认为,氢气是一种高效而无污染的理想能源,近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是。(选填字母)
| A.电解水 | B.锌和稀硫酸反应 |
| C.光解海水 | D.分解天然气 |
(2)用水分解获得氢气的能量变化如图所示,表示使用催化剂是曲线。该反应为(放热还是吸热)反应。
(3)1g的氢气完全燃烧生成液态水释放出142.9kJ的热量.写出其完全燃烧的热化学方程式:。
(4)氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验: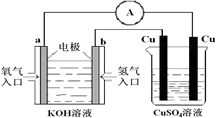
上图装置中,某一铜电极的质量减轻 6.4g ,则 a 极上消耗的O2在标准状况下的体积为L。
某化工集团为了提高资源利用率减少环境污染,将钛厂、氯碱厂和甲醇厂组成产业链。其主要工艺如下: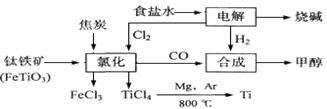
(1)写出工业上电解食盐水反应的化学方程式。
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式:。
(3)已知:①Mg(s) +Cl2(g)=MgCl2(s);ΔH=-641 kJ·mol-1
②Ti(s)+2Cl2(g)=TiCl4(s);ΔH=-770 kJ·mol-1
则2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s);ΔH=,反应2Mg+TiCl4 2MgCl4+Ti在Ar气氛中进行的理由是。
2MgCl4+Ti在Ar气氛中进行的理由是。
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中正极上的电极反应式是,负极区的pH(填“增大”、“减小”、“不变”)。
采用32%~35%的FeCl3溶液腐蚀印刷线路板上的金属铜,腐蚀废液中主要含有CuCl2、FeCl2和HCl等溶质。
(1)用FeCl3溶液溶解印刷线路板上金属铜的化学方程式为。
(2)工业上用铁粉回收腐蚀废液中的铜,方法如下:
①用铁粉回收铜的操作为:加入过量铁粉,充分搅拌,过滤、洗涤、。
②科学家对铁置换铜的工艺有如下研究:
分别在a、b、c三种条件下回收腐蚀废液中的铜,取充分反应后的粉末各3.000 g分别放入甲、乙、丙三个烧杯中,再加入100 mL 0.5mol·L-1的硫酸,水浴加热(70 ℃),搅拌,进行除铁处理。分别在第10、20、30、40、50 min时,用吸管移取0.5 g左右的铜试样于试管内,测定铜粉中铁的含量(质量分数),其结果如下图所示。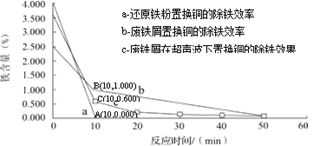
你认为除铁效果最好的是(填“a”、“b”或“c”),其原因是。
(3)工业上可用腐蚀废液制备CuCl2·2H2O,从而进行对废液的利用,其工艺流程如下: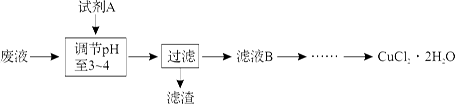
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
| 开始沉淀 |
2.3 |
7.5 |
4.7 |
| 完全沉淀 |
4.1 |
9.7 |
6.7 |
试剂A最好应选用(填写字母代号),理由是。
a.浓硫酸 b.Cl2c.NaClOd.NaOH溶液