25℃时,现有浓度均为0.10 mol/L的两种溶液:① (NH4)2SO4溶液、② Na2SO4溶液。请回答:
(1)两种溶液中,pH<7的是 (填“①”或“②”),其原因是 (用离子方程式表示)。
(2)下列说法正确的是 (填序号)。
① (NH4) 2SO4是弱电解质
② (NH4) 2SO4和Na2SO4均能促进水的电离
③两种溶液等体积混合后,溶液中离子浓度大小关系为:c(Na+)= c(SO42-)>c(NH4+)>c(H+)>c(OH-)
气体A由C、H、S、F中的三种元素组成,取标准状况下的1.12 L气体A装入一个薄膜里,袋和气体的总质量为2.20 g(不考虑浮力)。根据上述数据完成下列问题:
(1)估算A的相对分子质量不会大于__________。
(2)该气体A中含不含S元素?__________。
(3)确定A的化学式为__________。
在常温下的密闭容器中充入一定量的CH4、O2和足量Na2O2,用电火花不断引燃,待反应完全后,恢复到原温度,容器内压强几乎为0。求:
(1)容器内CH4和O2的物质的量之比应为__________。
(2)若容器中Na2O2的质量为23.4 g,则容器中O2的质量m的范围为__________。
一定质量的甲烷和氧气的混合气体,点燃后的产物有二氧化碳、一氧化碳和水,质量共为49.6 g,将燃烧后的产物缓慢地通过足量的无水氯化钙,氯化钙的质量增加了25.2 g,通过计算完成下列问题:
(1)在原混合气体中,甲烷和氧气的质量各为___________、___________克。
(2)在燃烧后的产物中,CO和CO2的质量各为___________、___________克
在120 ℃,101 kPa条件下,由H2、CH4、CO组成的混合气体a mL,通入一定量(设为x mL)氧气使其完全燃烧。
(1)若a mL混合气体完全燃烧后消耗相同条件下氧气的体积也为a mL(即x="a" mL),则原混合气体中CH4的体积分数是_________。
(2)若完全燃烧后生成CO2和H2O(g)的总体积在相同条件下为2a mL,则原混合气体中CH4的体积分数是_________。现要测定原混合气体中H2的体积分数,还必须知道相同条件下的其他数据,它们可以是_________ (填选项字母)。
A.2a mol混合气体的密度
B.生成CO2气体的总体积
C.生成H2O(g)的总质量
(3)若原混合气体完全燃烧所得气体中只有CO2和H2O(g),则x的取值范围是_________。
“立方烷”是一种新合成的烃,分子为正立方体结构,碳架结构如下图所示: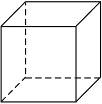
(1)“立方烷”的分子式为_________。
(2)该立方烷的二氯代物同分异构体的数目是__________。