用铝制饭盒盛放醋酸,一段时间后,饭盒被腐蚀,该种腐蚀属 ,反应的电极反应式为 。若用铝制饭盒盛放食盐(含水时),一段时间后,饭盒被腐蚀,这种腐蚀叫做 ,反应原理是(写电极反应式) 。
有A、B、C、D、E5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是________,B是________,C是________,D是________,E是________
(2)由这五种元素组成的一种化合物是(写化学式)__________。
写出该物质的一种主要用途____________________________
(3)写出C元素基态原子的电子排布式_________________________
(4)用轨道表示式表示D元素原子的价电子构型____________________
(5)元素B与D的电负性的大小关系是___________,C与E的第一电离能的大小关系是___________。(填“﹥”、“﹤”或“﹦”)
下表是元素周期表的一部分:
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅧA |
| 1 |
① |
||||||
| 2 |
② |
③ |
④ |
⑤ |
⑥ |
||
| 3 |
⑦ |
⑧ |
⑨ |
⑩ |
(1)表中元素⑩的氢化物的化学式为,此氢化物的还原性比元素⑨的氢化物的还原性(填强或弱)
(2)某元素原子同一能层中p能级电子数比s能级电子数少1,则该元素的元素符号是
(3)俗称为“矾”的一类化合物通常含有共同的元素是
(4)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式
又如表中与元素⑦的性质相似的不同族元素是(填元素符号)。
A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的原子结构示意图为;
(3)D元素的正三价离子的3d亚层为半充满,其二价离子的电子排布式为
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E基态原子的电子排布式为。
下表列出了前20号元素中的某些元素性质的有关数据:
| 元素编号 元素性质 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
| 原子半径(10-10m) |
1.52 |
2.27 |
0.74 |
1.43 |
0.77 |
1.10 |
0.99 |
1.86 |
0.75 |
0.71 |
| 最高价态 |
+1 |
+1 |
—— |
+3 |
+4 |
+5 |
+7 |
+1 |
+5 |
—— |
| 最低价态 |
—— |
—— |
-2 |
—— |
-4 |
-3 |
-1 |
—— |
-3 |
-1 |
试回答下列问题:
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是(填写编号)
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式),某元素R的原子半径为1.02×10-10m,该元素在周期表中位于,若物质Na2R2是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式。
在元素周期表中,元素的金属性和非金属性及其强弱比较与周期数(n)和主族数(A)有如下经验公式:K=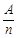 (K为A与n的比值)。请用编号回答下列问题:
(K为A与n的比值)。请用编号回答下列问题:
A.两性B.金属C.非金属D.稀有气体
(1)当n一定时,K值越大,则元素的_____性越强
(2)当A一定时,K值越小,则元素的_____性越强
(3)当K=0,则该元素系_____元素,当K=l时,则该元素系_____元素,当K<1时,则该元素系____元素。