尖晶石型锰酸锂(LiMn2O4)是一种环保绿色能源新型材料。实验室通过下列方法制取:将MnO2和Li2CO3按4︰1的物质的量比配料,球磨3~5小时,然后升温至600℃~750℃,保温24小时,自然冷却至室温得产品。
(1)保温24小时的目的是____________________________________________________。
(2)写出该反应的化学方程式_________________________________________________。
(3)实验室测定锰酸锂中锰的平均化合价的实验步骤如下:
步骤1:准确称取0.1g左右的尖晶石型锰酸锂试样于锥形瓶中,加入5mL稀硫酸、10.00mL 0.2000mol/L草酸钠(Na2C2O4)标准溶液,于80℃水浴加热溶解;
步骤2:待试样全部溶解,立即用浓度为0.2000mol/L的高锰酸钾溶液滴定至终点;
步骤3:计算样品得电子的物质的量n;
步骤4:将溶液中Mn2+氧化为Mn3+,再用硫酸亚铁铵标准溶液滴定,记录实验数据,计算出样品中Mn元素的质量为m;
步骤5:将实验步骤1-4重复2次。
已知反应: 2Mn3++C2O42-=2Mn2++2CO2↑;Mn4++C2O42-=Mn2++2CO2↑
2MnO4-+5C2O42-+16H+="2" Mn2++10 CO2↑+8H2O
①步骤2中,为判断滴定终点,_________(填“需要”或“不需要”)加入指示剂。
②步骤4中,滴定时盛放硫酸亚铁铵标准溶液的玻璃仪器是___________________。
③请用样品得电子的物质的量n和样品中Mn元素的质量m来表示样品中Mn元素的化合价=_____。
为测定氯化亚铁和氯化铁的混合物中铁元素的质量分数,某研究小组设计了如下两种实验流程:
(1)操作Ⅱ、Ⅲ是否完全相同?________(填“是”或“否”);操作Ⅳ使用的一种主要硅酸盐材料的仪器名称是________。
(2)甲方案中沉淀A是_______(填化学式);如何判断沉淀A洗涤干净? ________________________________________________________________________。
(3)乙方案中能否用铁粉做还原剂,请用文字说明理由____________________________。
(4)写出乙方案中滴入KMnO4溶液后发生反应的离子方程式_______________________。
(5)若甲方案中红棕色固体质量为bg,乙方案滴定时消耗c mol·L-1 KMnO4溶液dmL,哪个方案测定出来的铁元素含量更准确?_______(填“甲方案”或“乙方案”);据此方案测出的铁元素的质量分数为_______(用字母表示)。
实验室采用
、A
的混合溶液与过量氨水反应制备
,主要流程如下:
(1)为使
、
同时生成沉淀,应先向沉淀反应器中加入(填"
"或"
"),再滴加另一反应物.
(2)如下图所示,过滤操作中的一处错误是.
(3)判断流程中沉淀是否洗净所用的试剂是.高温焙烧时,用于盛放固体的仪器名称是.
(4)无水
(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备.
装置
中盛放饱和
溶液,该装置的主要作用是.
中试剂的作用是.用一件仪器装填适当试剂后也可起到
和
的作用,所装填的试剂为.
苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,反应原理: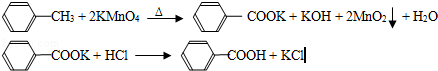
实验方法:一定量的甲苯和
溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.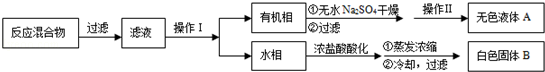
已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3
和6.9
;纯净固体有机物都有固定熔点.
(1)操作Ⅰ为,操作Ⅱ为.
(2)无色液体
是,定性检验
的试剂是,现象是
(3)测定白色固体
的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与
的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容.
| 序号 |
实验方案 |
实验现象 |
结论 |
| ① |
将白色固体 加入水中,加热溶解, | 得到白色晶体和无色溶液 |
|
| ② |
取少量滤液于试管中, | 生成白色沉淀 |
滤液含 |
| ③ |
干燥白色晶体, | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220 产品,配成100 甲醇溶液,移取25.00 溶液,滴定,消耗 的物质的量为2.40×10﹣3 ,产品中苯甲酸质量分数的计算表达式为,计算结果为(保留二位有效数字).
碘在科研与生活中有重要作用,某兴趣小组用
、0.2%淀粉溶液、
、
等试剂,探究反应条件对化学反应速率的影响.
已知:
(慢)
(快)
(1)向
、
与淀粉的混合溶液中加入一定量的
溶液,当溶液中的 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,
与
初始的物质的量需满足的关系为:n(
):n(
).
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验 序号 |
体积V/ml |
||||
|
溶液 |
水 |
溶液 |
溶液 |
淀粉溶液 |
|
| ① |
10.0 |
0.0 |
4.0 |
4.0 |
2.0 |
| ② |
9.0 |
1.0 |
4.0 |
4.0 |
2.0 |
| ③ |
8.0 |
Vx |
4.0 |
4.0 |
2.0 |
表中Vx=ml,理由是.
(3)已知某条件下,浓度c(
)~反应时间t的变化曲线如图13,若保持其它条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(
)~反应时间t的变化曲线示意图(进行相应的标注).
(4)碘也可用作心脏起捕器电源﹣锂碘电池的材料,该电池反应为:
已知:
则电池反应的
=;碘电极作为该电池的极.
现拟用图所示装置(尾气处理部分略)来制取一氧化碳,并用以测定某铜粉样品(混有
粉末)中金属铜的含量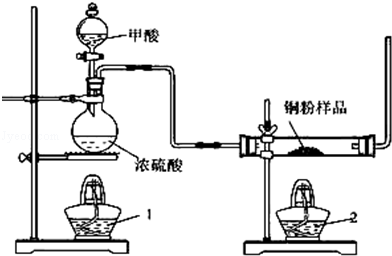
(1)制备一氧化碳的化学方程式是;
(2)试验中,观察到反应管中发生的现象是;尾气的主要成分是;
(3)反应完成后,正确的操作顺序为(填字母)
a.关闭漏斗开关 b.熄灭酒精1 c.熄灭酒精灯2
(4)若试验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,则原样品中单质铜的质量分数为;
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样品中金属铜质量分数的方案;
①设计方案的主要步骤是(不必描述操作过程的细节);
②写出有关反应的化学方程式.