A、B、C、D是短周期元素形成的四种气体单质。E、F均为气体,且F为红棕色。有关的转化关系如下图所示(反应条件均已略去)。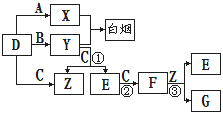
请回答下列问题:
(1)D的化学式为 、Y的化学式为 、E的化学式为 . (2)反应③的离子方程式为 。
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(4)0.1 mol·L-1的X溶液和0.1 mol·L-1的Y溶液等体积混合,溶液呈 ___性(填“酸”、“碱”或“中”),原因是_________ ____(用离子方程式说明)。
(18分)通过对模型、图形、图表的观察,获取有关信息是化学学习的一种重要能力。
(1)如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。按要求回答问题: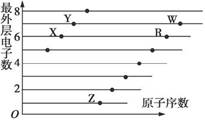
①Y元素在元素周期表中的位置为__________。
②气态氢化物的稳定性:X_____(填“>”“<”)Y。
③这五种元素形成的简单离子中,离子半径最大的是_______(填离子符号)。
④Z的氢化物ZH可以和水发生氧化还原反应,其反应方程式为_____________。
(2)X、Y、Z三种物质有以下转化关系: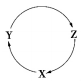
①如果三种物质中均含Mg元素,且X为镁单质,则Y、Z可能是_____、_______(填化学式,只填一种物质即可,下同);
②如果三种物质中均含Cl元素,且X为Cl2,则Y、Z可能是_____、______;
③如果三种物质中均含Si元素,且X为SiO2,则Y、Z可能是_____、______。
(3)向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,生成沉淀质量m与Ba(OH)2体积V之间的关系,则oa段生成的沉淀为____(填化学式,下同),ab段生成的沉淀为_____;bc段生成的沉淀为_________。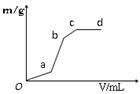
(15分)要准确掌握化学基本概念和研究方法。按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表:
每组分类均有错误,其错误的物质分别是_______(填化学式,下同)、_______、______。
(2)胶体和溶液的本质区别是______;鉴别胶体和溶液所采用的方法是观察是否能发生__________现象。
(3)下列3个反应,按要求填写相关量。
①2Na2O2 + 2H2O == 4NaOH + O2↑反应中,每消耗1mol Na2O2生成_______g O2;
②2NaHCO3=Na2CO3+H2O+CO2↑反应中,每消耗168g NaHCO3,标况下生成___L CO2;
③Cl2+H2O=HCl+HClO反应中,标况下每消耗22.4L Cl2,转移_____mol电子。
(4)在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,按要求回答下列问题: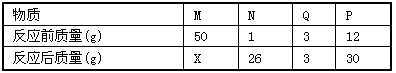
①该变化的基本反应类型是________反应; ②物质Q在反应中起的作用是_______。
(8分)标准状况下,进行甲、乙、丙三组实验,各取30.0 mL相同浓度的盐酸,然后分别慢慢地加入不同质量的同一种镁铝合金粉末,得下列有关数据(假设反应前后溶液的体积不发生变化):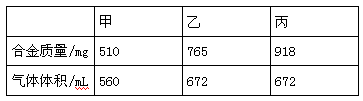
根据实验数据,计算:
(1)盐酸中HCl的物质的量浓度为_____________。
(2)合金中镁的质量分数(计算结果保留至0.1%,有必要的计算步骤和语言叙述,只写答案不得分,下同)。
(3)甲组实验后,还需向容器中加入lmol·L-1的NaOH溶液多少毫升恰好使铝元素以[Al(OH)4]-存在,并使Mg2+刚好沉淀完全?
(9分)A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系: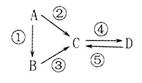
(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质。其中D与水反应生成酸的名称为______________。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。写出③反应的化学方程式__________。
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的气体。写出④反应的离子方程式_______________。
(4)若A是制造整流器和太阳能电池的材料。C、D为钠盐,两种物质中除钠、氧外的另一种元素为同一主族,且溶液均显碱性。写出②反应的化学方程式__________。
(5)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。写出④反应的离子方程式___________。
(8分)已知溶液中:还原性HSO3->I-,氧化性IO >I2>SO42-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。
>I2>SO42-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。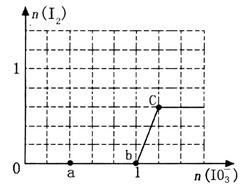
试回答下列问题:
(1)写出a点反应的离子方程式____________;反应中还原剂是_______;被还原的元素是________。
(2)写出b点到c点反应的离子方程式_______________。
(3)若往100mL 1 mol·L-1的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为__________。