在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是1 L“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
| 成分 |
质量(g) |
摩尔质量(g ·mol-1) |
| 蔗糖 |
50.00 |
342 |
| 硫酸钾 |
0.50 |
174 |
| 阿司匹林 |
0.35 |
180 |
| 高锰酸钾 |
0.50 |
158 |
| 硝酸银 |
0.04 |
170 |
(1)下列“鲜花保鲜剂”的成分中,属于强电解质的是________。
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为________________ mol/L。(只要求写表达式,不需要计算)
(3)配制上述1 L“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、________________、______________、_______________。(在横线上填写所缺仪器的名称)
(4)在溶液配制过程中,下列操作对配制结果没有影响的是___________。
A、定容时俯视容量瓶刻度线
B、容量瓶在使用前未干燥,里面有少量蒸馏水
C、容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D、定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
实验室可用碳酸钠制备少量亚硫酸钠晶体,有关装置如下图所示: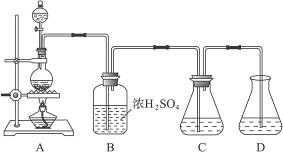
将17 g Na2CO3溶于80 mL水中,分装在C、D两个锥形瓶中,再将25 g铜屑放入圆底烧瓶中,将60 mL浓H2SO4和10 mL水的混合液装在分液漏斗中,逐滴加入硫酸后,小心加热使SO2逐渐产生(注意控制气量大小和反应速率的快慢)。将SO2通入Na2CO3溶液中至饱和,在合并C、D两瓶所得溶液中,慢慢加入17 g Na2CO3,蒸发浓缩,冷却后得亚硫酸钠晶体。试回答:
(1)如何配制60 mL浓H2SO4与10 mL水的混合液?
(2)装置B中浓H2SO4的作用:______________________________________________________;
(3)Na2SO3溶液要分装在两个锥形瓶中的理由是__________________;写出C中发生反应的离子方程式__________________;
(4)控制SO2产生速度的方法是_____________________________________________;
(5)通SO2结束后,加Na2CO3的目的是____________________________________。
下图虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,填写下列空白。
(1)如下图将装置中①②③三部分仪器的连接顺序变为②①③,则可以检验出的物质
是___________;不能检验出的物质是___________。
(2)如果将仪器的连接顺序变为①③②,则可以检验出的物质是___________;不能检验出的物质是___________。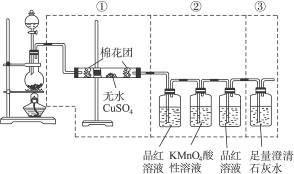
(3)如果将仪器的连接顺序变为②③①,则可以检验出的物质是___________;不能检验出的物质是___________。
写出CO2气体与Na2O2反应的化学方程式。某学生欲通过实验来探索SO2和Na2O2反应的产物,请你协助完成下列假设与设计:
(1)从SO2和Na2O2双方的性质出发,推测彼此反应的产物,写出虚拟反应式。
(2)画出完成此项实验的装置图。
(3)说明装置各部分所起的作用或添置它的目的。
(4)如何确认二者反应的产物?
图8-3是某气体X产生并研究其性质的装置。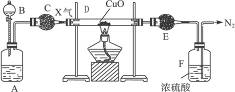
图8-3
A中盛有微溶的白色固体,B中盛有无色挥发性液体,C和E中盛有干燥剂。A和B中物质相遇时有无色气体X生成,它经图中一系列装置在末端得到N2,且E管的质量增加。
(1)写出盛放试剂的名称:
A.____________,B.____________,C.____________,E.____________。
(2)A和B中物质相遇生成X的主要原因是:________________________。
(3)D中反应的化学方程式_________________________________________。
(4)F中反应的化学方程式_________________________________________。
(5)从D中反应说明气体X具有____________(填“酸性”“碱性”“氧化性”或“还原性”)。
某研究性学习小组对氨气的制法进行了如下设计:
(1)下面是该小组同学提出的实验室制备氨气的几种方案:
A.硝酸铵固体与氢氧化钠固体共热
B.加热分解NH4Cl晶体
C.将浓氨水逐滴加到新制的生石灰中
你认为其中较为简便易行的方案有_______________(填写字母);其反应的化学方程式为__________________________________。
请从上图的仪器中选择制取氨气的发生装置(要求仪器少、合理)__________(写编号)。
(2)该小组需收集干燥后的氨气:
①如选用如右图所示的装置,则气体应由导管口_______(填“X”或“Y”)导入(集气瓶不能颠倒)。
②若用排液集气法收集氨气,可选用的试剂是_______(填字母)
A.H2O B.浓H2SO4C.CCl4 D.NaCl饱和溶液
(3)用图示装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是___________
________________________。
(4)若原烧瓶中氨气是充满的,进行喷泉实验后,烧瓶内溶液中溶质的物质的量浓度为_________(假定在标准状况下)。