、请回答下列问题。
(1)钢铁的电化学腐蚀原理如图所示:写出石墨电极的电极反应式_____________________;

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下:

①A电极的电极反应式是________________________。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为4.48 g,则电镀时电路中通过的电子为________ mol。(3)如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
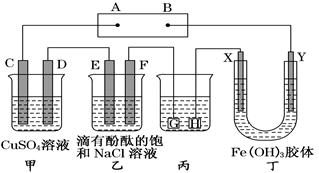
请回答:
①若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为________。
②当乙中溶液的pH是13时(此时乙溶液体积为500 mL),甲中溶液的pH为________。
③丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这种现象称为 ________
④乙中发生的反应方程式为:________________________。
X、Y、Z、W、T是原子序数依次增大的前四个周期的元素,其中有两种是金属元素。其相关信息如下表:
| 元素 |
相关信息 |
| X |
X一种核素在考古时常用来坚定一些文物的年代 |
| Y |
Y基态原子的s轨道电子与P轨道电子数相等 |
| Z |
Z是所在周期的单核离子中半径最小 |
| W |
W的单质被誉为“信息革命的催化剂”常用做半导体材料 |
| T |
T有多种化合物,其白色氢氧化物在空气中会迅速变为灰绿色,最后变为红褐色 |
(1)X、Y、Z三种元素的电负性由大到小的顺序是________(用元素符号表示,下同);在H-X、H-Y两种共价键中,键的极性较大的是。
(2)T2+的电子排布式为_________;T的单质在高温下与Y的氢化物反应,其化学方程式为;工业上用W的氧化物与X的单质高温下反应制得W单质的粗产品,其化学反应方程式为
(3)两种氢化物X2H2和H2Y2沸点相差很大,其沸点较高的是_______________,两者沸点相差很大的原因是____________________________________。
(4)在25℃、101 kPa下,已知W稳定的气态氢化物在Y的气态单质中完全燃烧,恢复至原来状态,平均每消耗4gW稳定的气态氢化物放热190.0KJ,则该反应的热化学方程式为 _____________。
化合物Ⅰ(C11H12O3)是制备液晶材料的中间体之一。Ⅰ可以用E和H在一定条件下合成:
已知以下信息:
A的核磁共振氢谱表明其只有两种化学环境的氢;
RCH=CH2 RCH2CH2OH
RCH2CH2OH
F是芳香族化合物,它的苯环上有四种氢,且取代基位置不相邻;
通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基( )。
)。
回答下列问题:
(1)A →B的反应条件_________。
(2)D与银氨溶液反应的方程式 _________。
(3)F的结构简式为___________,H中含氧官能团的名称
(4)E与H生成I的化学方程式为,该反应类型为__________。
(5)I的同系物J比I的相对分子质量小28,J的同分异构体中能同时满足如下条件:
①苯环上只有两个取代基;
②既能发生银镜反应,又能和饱和NaHCO3溶液反应放出CO2,共有种(不考虑立体异构)。
(6)分子式为C5H10O2的化合物K可做香料,分类时可以与I看作一类物质。该化合物在一定条件下可以水解成两种相对分子质量相等的有机物,其中一种可以发生催化氧化生成醛,写出符合条件的K的结构简式。
下图中的每1方格表示一种有关的反应物或生成物。其中A、C为无色气体。
完成下列问题:
(1)物质M可以是,F是。
(2)反应①除生成D外,生成的另一种物质的水溶液显碱性,用离子方程式解释溶液显碱性的原因:。
(3)检验M中阳离子的方法:。
(4)G到E的离子反应方程式:,每生成标况下1.12L的E,转移电子 mol。
A、B、D、E、F、G为短周期元素,且原子序数依次递增。A、F同主族,E、G同主族。A与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且F+与E2-核外电子排布相同,B是形成化合物种类最多的元素。
请回答以下问题:
(1)G在周期表的位置;
(2)写出D元素单质的电子式
(3)E、F形成的既有离子键又有共价键的化合物与A2E反应的方程式;
(4)B、D、E氢化物的稳定性从大到小的顺序(用化学式表示,下同): ;
E、G所在主族最高价氧化物对应水化物酸性最强的是,某种金属与其浓溶液在加热条件下可以得到一种蓝色溶液,用惰性电极电解该溶液时,阳极的电极反应式______________________;
(5)由A、B组成的化合物中,含A量最高的物质的化学式是。
研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
①已知:Fe2O3(s) + 3C(石墨) =" 2Fe(s)" + 3CO(g)△H 1 =" +489.0" kJ·mol-1
C(石墨) +CO2(g) = 2CO(g)△H 2 =" +173.0" kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为。
②某含C、H、O三种元素的有机物A,经测定碳的质量分数为52.16%,氢的质量分数13.14%,它可以作燃料电池(以KOH溶液为电解液)的原料,写出该电池的负极反应式。
(2)某实验将CO2和H2充入一定体积的密闭容器中,发生反应:
CO2(g) +3H2(g)  CH3OH(g) +H2O(g)△H =-49.0 kJ·mol-1
CH3OH(g) +H2O(g)△H =-49.0 kJ·mol-1
回答问题:
①该反应的平衡常数表达式为。
②把0.5mol的CO2和1.5mol的H2充入2L的密闭容器中,半分钟后测得c(H2)=0.15mol/L,用CH3OH表示该反应的速率:v(CH3OH)=
③如图,在反应体系中加入催化剂,反应速率增大,E2的变化是(填“增大”, “减小”或“不变”)