随着人们生活水平的提高,人们对于食品不但要求营养,更要求健康。市场上出现了一些不添加防腐剂的绿色食品,这种食品中有一个单独包装的保鲜剂,不会危害食品安全。某同学找来一种在空气中放置一段时间的食品保鲜剂,对它进行探究。
【查找资料】
(1)食物腐败是因为微生物在食物上生长。如右图所示,微生物只要得到养分,再加上充足的氧气和水,在适当的条件下就会迅速生长。因此,只要缺少一种条件,就可以防止食物腐败。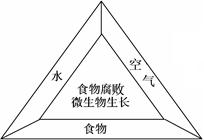
(2)常见的具有吸水性的物质有以下几种:
①浓硫酸 ②生石灰 ③氢氧化钠固体 ④铁粉
⑤硅胶(化学式SiO2●nH2O,无色透明粒状固体,无毒无害)
【活动与探究】
(3)初步探究:你认为①~⑤的物质中,不适合做食品干燥剂的是 ,理由是 。
(4)实验探究:
| 实验 |
操作 |
主要现象 |
结论与解释 |
| 实验1 初步判断 |
打开这种保鲜剂的包装袋,取少量样品于试管中,进行观察。 |
该样品为白色固体。 |
该保鲜剂一定不是 |
| 实验2 对该保鲜剂的有效性进行探究 |
向实验1的试管中加入适量的水,振荡。 |
形成白色浑浊液体, 试管壁发热。 |
结论与相关反应方程式 。 |
| 实验3 对该保鲜剂的成分进行探究 |
过滤实验2所得液体,向滤液中通入二氧化碳。 |
溶液变浑浊。 |
该保鲜剂中一定含有的物质是 ,对于实验3不能确定的物质是 。 |
| 将滤渣放入另一试管中,加入足量稀盐酸。 |
有气泡产生。 |
【活动反思】
(5)对于实验3不能确定的物质,某同学经过仔细研究,认为直接取原固体滴加酚酞溶液,通过观察颜色变化即可确定是否含有该物质,你认为这种方法是否合理?说明理由 。
(6)请根据食物腐败的条件分析,我们除可以使用这些保鲜剂外,还可以采用的保鲜方法是 。(写出一种即可)
实验室常用的干燥剂分碱性、酸性、中性三种类别。碱石灰是一种常用的碱性干燥剂,其成分为 和 ,它吸水能力强,不能干燥二氧化碳气体,在实验室应密封保存。
【学习交流】碱石灰不能干燥二氧化碳气体的原因分析
原因一:氢氧化钠与二氧化碳反应生成碳酸钠;
原因二: 。
实验室有一瓶因敞口久置后变质的碱石灰,某化学兴趣小组对其成分展开讨论与探究:
【提出猜想】变质的碱石灰除含水以外,可能还含有哪些成分?
猜想一:
猜想二:
猜想三:
猜想四:
猜想五:
【提出质疑】
兴趣小组部分同学认为猜想 不合理,应改为 。
【查阅资料】兴趣小组为了更好地进行实验探究,将常见盐的水溶液的酸碱性整理如下:
|
氯化钠 |
硝酸钠 |
碳酸钠 |
氯化钙 |
硝酸钙 |
氯化钡 |
硝酸钡 |
硫酸铜 |
|
中性 |
中性 |
碱性 |
中性 |
中性 |
中性 |
中性 |
酸性 |
【实验探究】
取少量碱石灰样品于试管中,加入足量蒸馏水。
(1)若发现样品完全溶解,则证明猜想 正确;
(2)若发现样品未完全溶解,过滤后得到滤渣M和溶液N,进行相关实验。
实验一:向溶液N中先滴加几滴酚酞溶液,可观察到溶液 ,仅根据此现象不能证明任一猜想是否正确,原因是 ,在此基础上,应如何设计实验证明猜想五正确?请写出实验操作及现象: 。
实验二:向滤渣M中加入适量盐酸,可看到有气泡产生,反应方程式为 。
【拓展延伸】干燥剂的选择要视被干燥气体的性质而定,碱性干燥剂不能干燥酸性气体,同理,酸性干燥剂不能干燥碱性气体。总之,干燥剂不能与被干燥气体发生化学反应。
小文研学旅行时,对“自热米饭”发热包的发热现象感到好奇。返校后,利用化学实验室中已有的生石灰、活性炭、铁粉、碳酸钠、氯化钠、硫酸钠中的若干种物质自制了一个发热包。发现使用自制发热包时,可迅速升温,还可保温较长时间。
小静同学对小文同学自制发热包的成分进行探究。
【实验探究】
小静取适量自制发热包中的固体放入盛有水的烧杯中,迅速放出大量的热,她认为是固体样品中的生石灰与水发生反应产生了热量。为了进一步确认发热包中物质的成分,小静把烧杯中的物质过滤,得到滤液A和滤渣B。
|
实验步骤 |
实验操作 |
实验现象 |
分析与结论 |
|
① |
取适量滤渣B放入烧杯中 |
观察到滤渣B慢慢出现红棕色固体,触摸烧杯外壁感到微热并持续了较长时间 |
红棕色固体是 |
|
② |
取适量滤液A放入试管中,加入过量的氯化钡溶液 |
有白色沉淀生成 |
发热包中除含有生石灰外,一定还含有的物质是 |
|
③ |
取②中的白色沉淀放入试管中,加入足量的稀硝酸 |
白色沉淀全部溶解,有气泡产生 |
|
|
④ |
取②反应后的上层清液放入试管中,先加入足量稀硝酸,再滴入适量 溶液 |
有白色沉淀生成 |
|
|
⑤ |
取适量滤渣B放入试管中,加入足量的稀盐酸 |
固体部分溶解,溶液呈浅绿色,有气泡产生 |
【反思与交流】
(1)步骤②反应后的上层清液中含有的离子共有 种。
(2)步骤④中生成白色沉淀的化学方程式是 。(任写一个)
(3)发热包中的物质使用前必须 保存,使用后注意合理回收。
实验活动课上,老师为大家演示兴趣实验,振荡留有小孔的盒子,将里面的黑色粉末均匀地洒在酒精灯火焰的上方,观察到火星四射的灿烂烟花。老师揭秘黑色粉末是食品包装袋中的脱氧剂。为此兴趣小组展开了对该脱氧剂成分及原理的探究。
实验活动一:探究脱氧剂中黑色粉末的成分。
【作出猜想】黑色粉末含有铁粉和碳粉中的一种或两种。
【实验探究】小组同学设计实验方案并完成如下实验:
|
实验步骤 |
实验现象 |
实验结论 |
|
①取黑色粉末放入烧杯中,加入稀盐酸。 |
,溶液变为浅绿色,有黑色不溶物。 |
黑色粉末中含有铁粉,反应的化学方程式为 。 |
|
②将①中黑色不溶物滤出,洗涤、干燥后,放在石棉网上灼烧,上方放一蘸有澄清石灰水的玻璃片。 |
。 |
黑色粉末中含有碳粉。 |
【查阅资料】实验所用脱氧剂中还含有氯化钠
实验活动二:探究脱氧剂中氯化钠的作用。
【实验探究】小组同学用控制变量法按如图装置进行实验:

一段时间后观察到烧杯内左侧导管液面 右侧导管液面(填“高于”或“低于”)。
【表达交流】脱氧剂利用铁生锈的原理延长食品保质期。其中碳粉具有 性,可以促进反应的发生,氯化钠可以加快铁生锈的反应速率。
实验活动三:探究溶液中溶质的成分。
【实验探究】小组同学用老师提供的完全变质的同种脱氧剂设计并完成如下实验:
|
实验步骤 |
实验现象 |
实验结论 |
|
①取适量完全变质的脱氧剂放入烧杯中,加入稀盐酸。 |
溶液由无色变为黄色,有黑色不溶物。 |
反应的化学方程式为 。 |
|
②取①中过滤后的滤液,向其中滴加少量氢氧化钠溶液。 |
无明显现象。 |
滤液中溶质的成分为 。 |
【反思评价】脱氧剂包装上应注明的注意事项是 (请写出一条)。
二氧化碳是人类生存不可缺少的物质,某兴趣小组利用如图装置对二氧化碳的性质进行以下探究。(夹持装置已省略)

(1)探究一:检查装置的气密性,打开 ,关闭 、 ,往B中加入药品。一段时间后观察到③处纸花先变红,①处纸花后变红,②处纸花不变色,说明二氧化碳能与水反应,该反应的化学方程式为 ,也能证明二氧化碳具有的物理性质是 。
(2)探究二:打开 ,关闭 、 ,C中出现浑浊,说明二氧化碳与氢氧化钙反应生成了碳酸钙。有同学质疑:白色固体可能是二氧化碳与水反应导致溶液中水减少而析出的氢氧化钙,小组同学向C中加入足量的水验证,白色固体不溶解,该方法利用了氢氧化钙和碳酸钙 (填具体性质)。
(3)探究三:打开 ,关闭 、 ,一段时间后,D中无明显现象。小组同学通过探究二的结论推理,二氧化碳能与氢氧化钠反应生成碳酸钠。为验证推理是否正确,进行了如下实验。
|
操作 |
现象 |
结论 |
|
向D反应后的溶液中加入足量的氯化钡溶液,振荡,观察现象 |
|
二氧化碳能与氢氧化钠反应生成碳酸钠 |
(4)废液处理:小组同学在对D试管的废液过滤后分类处理时,测得滤液显碱性,故向滤液中加入稀盐酸调节酸碱度,发现滴入盐酸时产生气泡,经检验该气体为二氧化碳,得出新的结论,探究三中二氧化碳与氢氧化钠反应除生成碳酸钠和水外,还生成 。
(5)依据二氧化碳的性质写出二氧化碳与氢氧化钾溶液反应的一个化学方程式: 。
小苏打在日常生活中常用于浸泡蔬菜以杀死虫卵,清除农药等。小苏打不稳定,受热易分解而变质( )。小明对厨房里的小苏打取样探究。
【做出猜想】猜想1:该样品是 ;猜想2:该样品是 ;
猜想3:该样品是 、 的混合物。
【查阅资料】① 受热不分解;②溶液中 与 不反应。
【定量探究】取该样品 g在一试管中充分加热至质量不再变化,冷却至初始温度称量,试管中物质质量为 g。
【讨论交流】测得 ,可以确定猜想 (填“1”“2”或“3”)不成立。
【定性探究】i.另取一定量该样品于烧杯中,加入足量 溶液,产生白色沉淀;
ii.待上述物质充分反应后过滤,向滤液中加入稀盐酸,产生气泡。
【反思与评价】
(1)实验i证明该样品中一定有 ,所发生反应的基本类型为 。
(2)根据实验i、ii,可以断定最初猜想 (填“1”“2”或“3”)正确,实验ii有关反应的化学方程式为 。
(3)实验中涉及过滤操作,下列有关说法正确的是 (填选项字母)。
a.使漏斗下段管口正对烧杯中央
b.玻璃棒末端斜靠在三层滤纸的一边
c.漏斗中滤纸边缘高于漏斗边缘
d.过滤器中的液面始终低于滤纸边缘