(18分)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)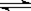 CH3OH(g)。
CH3OH(g)。
(1)分析该反应并回答下列问题:
①平衡常数表达式为K=__________________。
②下列各项中,不能够说明该反应已达到平衡的是________(填序号)。
A、恒温、恒容条件下,容器内的压强不发生变化
B、一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
C、一定条件下,CO、H2和CH3OH的浓度保持不变
D、一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
(2)下图是该反应在不同温度下CO的转化率随时间变化的曲线。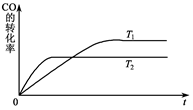
①该反应的焓变ΔH________0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”)。
③若容器容积不变,下列措施可增加甲醇产率的是________。
A、升高温度
B、将CH3OH(g)从体系中分离
C、使用合适的催化剂
D、充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。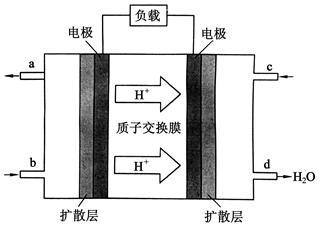
①该电池工作时,b口通入的物质为______________,c口通入的物质为_____________。
②该电池正极的电极反应式为:________。
③工作一段时间后,当6.4 g甲醇完全反应生成CO2时,有_____________NA个电子转移。
(1)某化学兴趣小组按照下列流程进行“由镁铝合金制备硫酸铝晶体”的实验。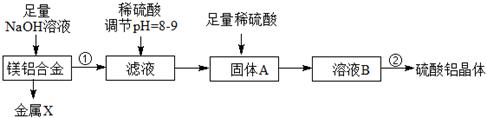
则镁铝合金中加NaOH溶液的化学反应方程式为,金属X是,
固体A的化学式,操作②包含的步骤有蒸发浓缩、、过滤、干燥。
(2)某兴趣小组为测定镁铝合金中各组成的质量分数,设计图示装置。则仪器甲的名称,需要测定的数据有。(已知该实验时的温度压强)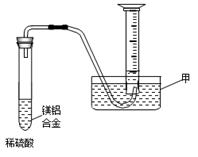
(3)现有一定量的AlCl3和FeCl3混合溶液,已知其中Al3+、Fe3+的物质的量之和为0.10 mol,若向此溶液加入170 mL 2mol/L NaOH溶液,设Al3+物质的量与总物质的量的比值为x。则x=0.4时,沉淀的物质的量为mol。请在图中画出沉淀总量(y mol)随x(0→1)变化曲线。
在下图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,F在D中燃烧发出苍白色火焰。H可用于制造光导纤维,J是一种乳白色凝胶状沉淀。(部分生成物和部分反应条件未列出)
请回答下列问题:
(1)A的电子式为。
(2)H的化学式为。
(3)写出反应①的离子方程式。
(4)写出反应②的化学方程式。
(1)食品和药品关系人的生存和健康。
①市场上销售的食盐品种很多。下列食盐中,所添加的元素不属于人体必需微量元素的是(填字母)。
A.加钙盐 B.加碘盐 C.加锌盐
②纤维素被称为“第七营养素”。食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排出有害物质。在化学分类中,纤维素属于(填字母)。
A.蛋白质 B.脂肪 C.多糖
③某同学感冒发烧,他可服用下列哪种药品进行治疗(填字母)。
A.麻黄碱 B.阿司匹林 C.抗酸药
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
① 在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其各成分金属的熔点。(选填“高”或“低”)
② 炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑。铁锅的腐蚀主要是由腐蚀造成的。
③ 石英玻璃纤维又称光导纤维,其主要成分和NaOH溶液反应的离子方程式为
。有机玻璃受热时会软化,易于加工成型。有机玻璃是一种材料(选填“橡胶”或“纤维”或“塑料”)。
(3)防治环境污染,改善生态环境已成为全球的共识。
① pH<5.6的雨水称为酸雨,主要是由人为排放的硫氧化物和等酸性气体转化而成的。向煤中加入石灰石作为脱硫剂,可以减少煤燃烧时产生的SO2。发生反应的化学方程式为。
②NaNO2作为食品添加剂不能大量食用,因为它会与肉类中的蛋白质反应生成致癌的化合物。CO使人中毒是因为很容易和人体血液中的结合。
③城市餐饮业会产生大量污染环境的“地沟油”。综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取甘油和。生活中会产生大量废弃塑料,将废弃塑料进行处理,可以获得乙烯、丙烯等化工原料。
取20 mL NaOH溶液平均分成两份,分别放入A、B两支试管中。向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如下表所示:
| 盐酸体积(单位:mL) |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
| A产生CO2的体积 |
0 |
0 |
0 |
0 |
0 |
22.4 |
44.8 |
44.8 |
44.8 |
| B产生CO2的体积 |
0 |
0 |
22.4 |
44.8 |
67.2 |
89.6 |
x |
x |
x |
请回答下列问题
(1)少量CO2与NaOH溶液反应的离子方程式,
过量CO2与NaOH溶液反应的化学方程式;
(2)试管A中通入CO2后所得溶液的溶质为;
(3)原NaOH溶液的物质的量浓度为mol/L;
(4)滴加70mL盐酸时,A、B产生CO2的体积均为最大值,则x=mL。
下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟生成E,A是强碱,D的焰色为紫色 (部分反应物和生成物及水已略去)。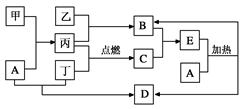
请回答下列问题
(1)写出工业制备B的化学方程式_____________________________________;
(2)写出常温下,A与丁反应的离子方程式________________________________;
(3)下图装置为用排空气法收集气体的实验装置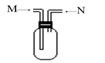
Ⅰ.当从M端通入气体时,可收集的气体有;
Ⅱ.当从N端通入气体时,可收集的气体有 ; (填数字编号)
①气体乙②气体丙③气体丁④气体B⑤气体C
(4)E中所含阳离子的检验方法为(包括实验步骤、现象及结论);
(5)A中所含阳离子的检验方法为(包括实验步骤、现象及结论)。