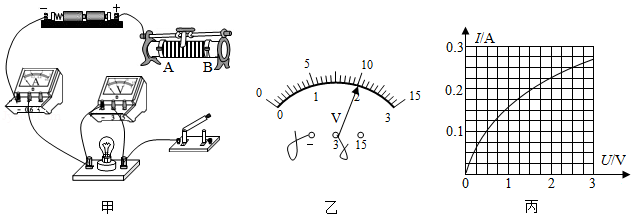
为确定某种未知液体的“身份”,物理老师把这个任务交给了小明的实验小组,他们利用天平和量筒进行了多次测量.某次的操作如下: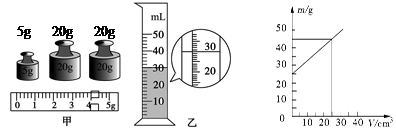
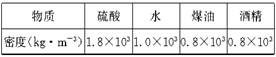
(1)用天平测量液体的质量.当天平平衡时,放在右盘中的砝码大小和游码的位置如图甲所示,则称得烧杯和液体的质量m为________g.
(2)用量筒测量液体的体积.将烧杯中的液体全部倒入量筒中,液面达到的位置如图乙所示,则该液体的体积V为_____mL.尽管体积测量方法正确,但大家在对实验过程及结果进行评估时,发现液体的体积测量值比它的实际值要_____(选填“偏大”或“偏小”).
(3)他们对测量方法进行修正后,测出了几组实验数据,并根据测量结果作出了“m-V”图象,如图所示.由图象可知该液体的密度为_____g/cm3;通过查表对照知该液体是________.
在“测量小灯泡的电功率”的实验中,实验室提供如下器材:电源(电压恒为
、电压表和电流表各一个、额定电压为
的待测小灯泡
(电阻约为
、滑动变阻器两个
:“
“;
:“
“
、开关
、导线若干。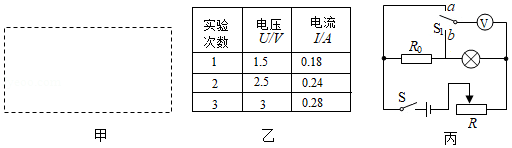
(1)该实验的原理是电功率 。
(2)实验中,应选用的滑动变阻器是 (选填“ ”或“ ” ;
(3)选用滑动变阻器后,请你根据以上器材设计一个测量小灯泡电功率的实验电路图,并画在图甲的虚线框内;
(4)某小组在实验中记录了3组小灯泡的电流随电压变化的情况,如图乙所示,完成实验后小组进一步求得该小灯泡正常发光时的电阻为 。(保留到小数点后一位)
(5)另一小组实验时,发现电流表已经损坏,为了测出该小灯泡的额定功率,小组在实验室选了一个 的电阻 和一个单刀双掷开关,设计了如图丙所示的电路并完成了该实验(电源电压不变)
①闭合开关 , 接 ,调节滑动变阻器 使小灯泡正常发光,记录电压表示数 。
②闭合开关 ,滑动变阻器滑片保持不动, 接 ,读出此时电压表示数为 。
则小灯泡额定功率 (用 、 、 表示)。
关于“阻力对物体运动的影响”问题,某学习小组进行了如下探究实验:依次将毛巾、棉布分别铺在水平木板上,让小车分别从斜面顶端由静止自由下滑,观察小车在水平面上滑行的最大距离,三种情况下的运动如图所示。
(1)实验中每次均让小车从斜面顶端由静止自由下滑,目的是使小车在水平面上开始滑行时获得的速度大小 (选填“相等”或“不相等” ,本实验中的“阻力”是指小车受到的 ;
(2)分析图运动情况可知:小车在毛巾表面上滑行的距离最短,说明小车受到的阻力越大,速度减小得越 (选填“快”或“慢” ;
(3)牛顿在伽利略等人的研究基础上,概括出牛顿第一定律:一切物体在没有受到力的作用时,总保持 状态或 状态;
(4)牛顿第一定律 (选填“是”或“不是” 直接由实验得出的,其符合逻辑的科学推理为科学研究提供了一个重要方法。
在“测定小灯泡额定功率”的实验中,电源电压为 ,小灯泡的额定电压为 。
(1)请在图甲中用笔画线代替导线,完成电路连接;

(2)闭合开关,在将滑动变阻器的滑片从一端缓慢移到另一端的过程中,发现电压表示数 与滑片移动距离 的关系如图乙所示,电压调节非常不方便,这是由于选用了以下提供的 (选填“ ”或“ ” 滑动变阻器;可供选用的滑动变阻器:滑动变阻器 (阻值范围 ,滑片行程 滑动变阻器 (阻值范围 ,滑片行程
(3)换用另一个滑动变阻器并接通电路后,移动滑片,当电压表的示数为 时,电流表的示数如图丙所示,则小灯泡额定功率为 ;
(4)小明想换用其他规格的小灯泡再做该实验,但他操作有误,在未断开开关的情况下,直接将小灯泡从灯座上拔出,那么拔出小灯泡后电压表的示数情况是 电流表的示数情况是 (以上两空选填“示数为零”或“有较大示数” ;
(5)实验完成后同学们在老师的提醒下结合图的电路图进行了误差 分析:因实验中实际提供的电压表内阻并非无穷大且在测量时有明显的电流通过,会造成电流表所测电流 (选填“大于”或“等于”或“小于” 灯泡中的实际电流,从而导致实验中灯泡额定功率的测量值 (选填“大于”或“等于”或“小于” 真实值。

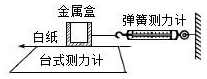
针对“滑动摩擦力大小是与压力有关,还是与重力有关?”这一问题,某物理兴趣小组的同学利用如图所示装置进行了探究,实验步骤和数据记录如表:
|
实验步骤 |
台式测力计示数 |
金属盒重力 |
弹簧测力计示数 |
|
|
① |
把金属盒放在质量不计的白纸上,在拉动白纸的过程中读出测力计的示数 |
4.8 |
4.8 |
1.9 |
|
② |
将质量不计的氢气球系在金属盒上,重复步骤①的实验 |
3.2 |
4.8 |
1.2 |
|
③ |
氢气球仍系在金属盒上,往金属盒加入适量的沙子,使台式测力计的示数为 ,再重复步骤步骤①的实验 |
4.8 |
6.4 |
1.9 |
(1)此实验是根据二力平衡原理 (选填“间接地”或“直接地” 测出摩擦力大小;
(2)实验步骤②使用氢气球是为了改变 (选填“金属盒对纸的压力”或“金属盒的重力” ;
(3)根据实验步骤②、③的数据 (选填“能”或“不能” 说明摩擦力大小与压力有关;
(4)要分析摩擦力大小与重力大小是否有关,应选择 两组数据进行分析;
(5)与直接用弹簧测力计拉动金属盒测量摩擦力相比,拉动白纸进行实验有许多优点,以下说法中不是其优点的是 (选填字母序号)。
.不需要匀速拉动白纸
.测力计位置和示数较稳定
.拉动白纸时所用拉力较小,能省力
在“测量小灯泡的电功率”实验中,实验器材有:两节新干电池、电流表、电压表、额定电压 的小灯泡,滑动变阻器、开关、导线若干,部分实物电路如图甲所示。
(1)请用笔画线代替导线,将图甲中的实物电路连接完整(要求:滑片 向右移动时小灯泡变亮)。
(2)连接好电路,闭合开关,发现小灯泡很亮,电压表示数为 .断开开关,经检查,各元件完好,电路连接正确则实验中操作错误之处是 。
(3)改正错误后进行实验,移动滑动变阻器的滑片到某一位置,电压表的示数如图乙所示;若要测量小灯泡的额定功率,滑动变阻器的滑片 应向 端移动(选填“ ”或“ ” 。
(4)图丙是由实验数据描出的小灯泡的 图象,则小灯泡额定功率是 。
(5)根据小灯泡的 图象计算出不同电压下灯丝电阻值不同,原因是灯丝电阻随 的变化而变化。
(6)若用第(3)小问中所测得数据算出灯泡的电阻 ,再根据 计算灯泡的额定功率。按此方案算出灯泡的额定功率比真实值 (选填“偏大”或“偏小” 。