某校同学选用下列装置制备二氧化碳气体,请回答下列问题: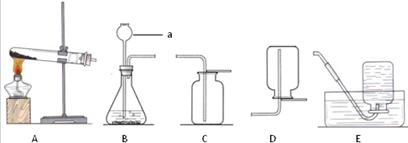
(1)仪器a名称 ;实验室制取二氧化碳常用药品 和
(2)实验室制取二氧化碳应选用的发生装置是 收集装置是 (都填字母序号)
(3)实验室用高锰酸钾制取氧气应选用的装置是 (填字母序号)
化学方程式是
在“质量守恒定律”的教学中,老师引导同学们进行“化学反应中反应物与生成物的质量关系”的实验探究,请你参与探究并回答有关问题:
(1)如图A、B所示,将锥形瓶(反应物未接触)放在天平上,右盘加砝码使之平衡,取下锥形瓶,将锥形瓶中两种物质混合,反应完全后将锥形瓶再放回天平左盘上。
①A瓶重新放回到天平上,天平(填“能”或“不能”)保持平衡。
②B瓶重新放回到天平上,天平能否保持平衡?,理由是。
③从原子的角度分析“质量守恒定律” 。
(2)如上图C所示,用细线系住镁条使之平衡,然后在镁条一端用酒精灯加热。镁条在加热的条件下,能与空气中的氧气反应生成氧化镁。
①写出镁在空气中加热的文字表达式。
②加热一段时间后,镁条(填“能”或“不能”)保持平衡。
(3)某同学利用如图所示的装置测定空气中氧气的含量(体积分数)。他的操作过程如下(有100mL和500mL量筒供选用):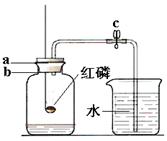
①检查整个装置的气密性后,将c处的止水夹夹紧,点燃红磷后,迅速插入左边的广口瓶中;
②待燃烧停止,整个装置冷却至室温后,将c处的止水夹打开。结果发现烧杯中的水进入到广口瓶中;
③待烧杯中的水不能再进入广口瓶后,打开广口瓶的橡胶塞,将广口瓶中的水全部倒入到100mL量筒中,测得其中水的体积为76ml。
④该同学又设法准确地测定了广口瓶中空气的体积,数据为400mL。
回答下列问题:①红磷燃烧时最明显的现象是___________________________;
②该同学测得的空气中氧气的体积分数为________%。与理论值21%相比较,产生误差的原因很可能是_____________________(导气管的体积可忽略不计)。
(6分)盐城是全国酸雨高发地区之一,某化学兴趣小组得知酸雨是因空气中的二氧化硫与水反应生成酸而导致,他们想对此进行探究,请你参与他们的探究过程:
(1)做出假设:;
(2)设计方案:用紫色的石蕊试液浸泡,制成紫色纸花并晾干。先验证水能否使紫色纸花变色,再验证二氧化硫气体能否使干燥的紫色纸花试纸变色,最后验证二氧化硫气体能否使湿润的紫色纸花变红,实验装置和药品如图:
(3)查阅资料:你认为该实验小组不需要掌握的资料内容中应包括(填序号);
①二氧化硫易溶于水②酸能使湿润的紫色石蕊试纸变红③SO2不与浓硫酸反应
(4)实验:①实验中纸花(Ⅱ)的颜色始终没有变化,这说明。
②纸花(Ⅲ)在实验过程中始终未见变色,此现象说明。
③实验Ⅰ的作用是。
(5)结论:实验过程中只有Ⅳ纸花变红,说明原假设(填“成立”或“不成立”)
某兴趣小组同学利用下图所示装置探究燃烧的条件。
【分析】(1)步骤①中白磷不燃烧的原因是。
(2)对比(填实验步骤的序号)可知燃烧需要氧气。
【结论】通过对实验分析,小组同学得出可燃物燃烧的条件是需要氧气、。
| 步骤 |
操作 |
现象 |
| ① |
打开K1,关闭K2 |
无明显现象 |
| ② |
打开K2,关闭K1 |
|
| ③ |
打开K2,关闭K1,将A中的液体滴入B中 |
C中有气泡冒出,白磷不燃烧 |
| ④ |
打开K1,关闭K2,将A中的液体滴入B中 |
D中有气泡冒出,白磷燃烧 |
【反思】(1)装置中的气球所起作用是。
(2)常言道“水火不相容”,但本实验步骤④中也观察到“水火相容”的奇观,其原因是。
Ⅰ.某研究性学习小组的同学学习了二氧化碳的性质后,对二氧化碳溶于水的过程,有没有发生化学变化?提出实验改进:用如图所示装置进行实验,验证二氧化碳能与水反应(已知氮气的密度小于空气的密度),
操作为:
①从a端通入二氧化碳
②从分液漏斗中滴加适量水
③从b端通入氮气
④将石蕊溶液染成紫色的干燥纸花放入广口瓶中
实验操作顺序最合理的是___,发生变化的化学方程式为。
Ⅱ.另一小组在课外活动时对“二氧化硫能否与水反应生成酸”进行了实验探究。请你参与他们的探究活动,并回答有关问题。
[查阅资料]常温下二氧化硫是一种无色气体,易溶于水。
[假设]二氧化硫能与水反应生成酸。
[设计实验]
(1)小雨同学将二氧化硫气体通入紫色石蕊试液中,观察溶液颜色的变化。他认为,若紫色石蕊试液变色,则证明假设成立。
(2)小涛同学认为小雨同学的实验方案不严密。小涛同学用紫色石蕊试液将白色滤纸染成紫色,干燥后做成三朵紫色的小花,然后按下列图示进行实验,在(I)、(Ⅱ)、(Ⅲ)中分别观察到变色和不变色的两种现象。
小涛同学认为,若(填序号)中的紫色小花变色,则证明假设成立。
[交流反思]小明同学对小涛同学的实验方案提出了质疑,他认为上述实验还不足以证明“二氧化硫和水反应生成了酸”,其理由是。三位同学讨论后补充了一个实验,使探究活动获得了成功,你认为这个实验应该是(简述实验步骤和现象)。
[结论]通过上述实验得出:二氧化硫能与水反应生成酸。
小明同学对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】
a.可能与硫酸的质量分数有关;
b.可能与锌的形状有关。
【查阅资料】
锌的化学性质比较活泼,在常温下的空气中,表面生成一层“保护膜”,可阻止进一步氧化。该“保护膜”可以和酸反应,但不产生氢气。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
| 实验编号 |
硫酸的质量分数(均取20mL) |
锌的形状(均取1g) |
氢气的体积(mL)(均收集3分钟) |
| ① |
20% |
锌粒 |
31.7 |
| ② |
20% |
锌片 |
50.9 |
| ③ |
20% |
锌粒 |
61.7 |
| ④ |
30% |
锌片 |
79.9 |
(1)写出稀硫酸与锌反应的化学方程式______________________________。
(2)小兵用图装置收集并测量氢气的体积,其中量筒的作用是_______________________,
氢气应从________(填e或f或g)管通入;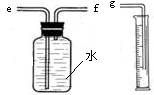
【收集证据】
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________;
【得出结论】
(4)结论是_____________________________________________________;
【评价与反思】
(5)下表是小兵第①组实验的详细数据。
| 时段(均为1分钟) |
第1分钟 |
第2分钟 |
第3分钟 |
第4分钟 |
第5分钟 |
第6分钟 |
| H2的体积 |
3.1mL |
16.7mL |
11. 9mL |
9.6mL |
7.6mL |
6.0mL |
请描述锌与硫酸反应的先慢后快最后又变慢的原因___________________________;
(6)你认为锌与硫酸反应的快慢可能还受因素影响?
(7)取某厂生产的生铁样品6g,与100g足量的稀硫酸充分反应后,称得剩余物质的总质量为105.8g。
①生成气体的质量为克;
②该厂生产的生铁样品中铁的质量分数是多少?(写出具体的过程,结果精确到0.1%)
③该厂生产的生铁是否合格?(填“合格”或“不合格”)