化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究。
【提出问题】金属与盐酸反应的剧烈程度受哪些因素的影响?
【做出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】实验所用的金属均已用砂纸打磨。
实验(1)为探究猜想a,小明同学分别在两支试管中放入相同质量的镁片和铁片,然后分别加入相同浓度和质量的稀盐酸,观察到放镁片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,写出镁与盐酸反应的化学方程式 。
从实验现象可以判断:金属活动性Mg Fe(填“>”“<”或“=”)。
得出结论: 。
实验(2)为探究猜想b,小组同学设计如图装置进行实验,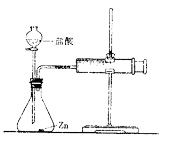
所用药品、实验数据如下表:
| 实验编号 |
选用金属 (均取2g) |
盐酸浓度(均取50ml) |
每30秒产生气体的体积/ml |
|||||
| 30秒 |
30-60 秒 |
60-90秒 |
90-120秒 |
120-150秒 |
前150秒共收集气体 |
|||
| Ⅰ |
镁片 |
10% |
2.9 |
16.9 |
11.9 |
9.2 |
7.6 |
48.5 |
| Ⅱ |
镁片 |
5% |
1.6 |
8.4 |
5.9 |
4.8 |
3.7 |
24.4 |
其中注射器的作用是 。
得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是 。
【反思评价】本题奖励4分,化学试卷总分不超过60分。
根据表中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因 。通过以上探究,你认为金属与盐酸反应的剧烈程度还可能受哪些因素影响,设计实验验证。 。
某研究小组对蜡烛及其燃烧实验进行了如下探究。
(1)探究一:把一根小木条平放入火焰中,约1s后取出,发现小木条的外端首先变黑,由此得到的结论是 _________ 。
(2)探究二:在火焰上方罩一个干冷烧杯,发现烧杯内壁产生水雾,说明蜡烛燃烧生。
(3)探究三:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由 _________ (填“固态”或“气态”)物质燃烧形成的。
(4)探究四:物质燃烧产生火焰的根本原因是什么?
查阅资料
| 物质 |
熔点╱℃ |
沸点╱℃ |
燃烧时温度╱℃ |
| 石蜡 |
50∽70 |
300∽550 |
约600 |
| 铁 |
1535 |
2750 |
约1800 |
| 钠 |
97.8 |
883 |
约1400 |
由上表可知:物质燃烧能否产生火焰与其 _________ (填“熔点”或“沸点”)和燃烧时温度有关,由此推测:钠在燃烧时, _________ (填“有”或“没有”)火焰产生。
小明家的电线晚上出了问题,几个电灯忽亮忽灭,忽明忽暗。爸爸说一定是电路中有接触不良的地方。他用干燥的木棍,轻轻不动屋檐下的电线,几经周折后才恢复了正常。
第二天,小明帮电工师傅一起查找线路故障,他们检查了电线的每一部位,直到检查到一铜线和铝线的接口处才发现了问题,他们发现上面“长满了”灰色、绿色的粉末。师傅说:“铝、铜的接口出容易生锈,问题往往出在这些地方。”小明对师傅的话半信半疑,又检查了一遍,确实是铜铝接口处生了锈,而铝、铝接口处和铜、铜接口处都没生锈,这是必然还是偶然原因造成的?只有铝、铜接口处生锈吗?不同金属接口处都易生锈吗?小明想通过实验弄明白这些问题,他找来铜丝、铝丝、铁丝、薪条,想研究模仿自然条件下,较长时间后导线接口出生锈情况。
请你和小明一起完成下列问题:
⑴怎样设计这个实验?请你简要写出实验步骤和操作方法。
。
⑵通过几个月的观察,若得出“只要是不同种类金属相连接,就比同种金属相连接易生锈”的结论。那么,上面所设计的实验在几个月后出现的现象应分别是。
⑶为避免类似小明家断电现象的发生,安装民用线路时请你给电工师傅提出建议。
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
①为探究催化剂的种类对双氧水分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g 10%H2O2溶液与1.0g MnO2均匀混合
Ⅱ.将x g10% H2O2溶液与1.0g CuO均匀混合
在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中反应的化学(符号)表达式是________;Ⅱ中x的值应为________。
②乙探究了影响双氧水分解速度的某种因素。实验数据记录如下:
| 双氧水的质量 |
双氧水的浓度 |
MnO2的质量 |
相同时间内产生O2体积 |
|
| Ⅰ |
50.0g |
1% |
0.1g |
9 mL |
| Ⅱ |
50.0g |
2% |
0.1g |
16 mL |
| Ⅲ |
50.0g |
4% |
0.1g |
31 mL |
本实验中,测量O2体积的装置是________(填编号)。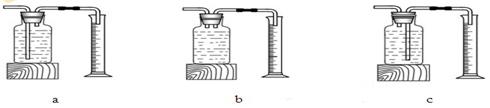
实验结论:在相同条件下,_______________,双氧水分解得越快.
丙用右图装置进行实验,通过比较___________也能达到实验目的。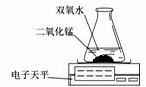
子涵根据燃烧红磷测定空气中氧气含量的实验原理,认为可用木条燃烧产生的木炭代替红磷测定空气中氧气的含量,并按右图装置进行实验。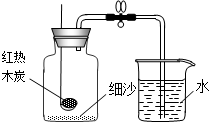
①依据的实验原理是 。
子涵检查装置气密性后,将盛有足量红热木炭的燃烧匙迅速伸入集气瓶中,并把塞子塞紧,待红热的木炭熄灭并冷却至室温后,打开弹簧夹,并未发现倒吸现象。经过认真分析,
子涵发现实验失败的原因是(答一条)。
②子涵将集气瓶中的细沙改为 溶液,重复上述①实验,有倒吸现象。子涵还发现倒吸的水量未达到集气瓶内原剩余容积的1/5。原因可能是(答一条)
。
③子涵反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是(答一条)。
实验探究对人体吸入的空气和呼出的气体有什么不同实验中:
(1)用的方法收集人体呼出的气体。
(2)实验步骤、现象及结论如下表
| 实验步骤 |
实验现象 |
分析现象及结论 |
| 取一瓶呼出的气体和一瓶空气,分别滴入澄清的石灰水,振荡 |
人体呼出的气体中,二氧化碳的含量高于空气中二氧化碳的含量。 |
|
| 取一瓶呼出的气体和一瓶空气, |
燃着的小木条在呼出的气体中立即熄灭,在空气的瓶中持续燃烧了一会儿再熄灭 |
人体呼出的气体中, 。 |
| 取两片干燥的玻璃片,其中一片放在空气中,向另一片呼气 |
人体呼出的气体中, 。 |
(3)此实验的探究方法是。