核内中子数为N的R2+,质量数为A,则该离子的核外电子数为
写出下列物质的电子式:
(1)MgCl2(2) CO2(3)NaOH(4) H2O2
、A、B、C、D、E均为有机化合物,它们之间的关系如图所示(提示:RCH=CHR'在酸性高锰酸钾溶液中反应生成RCOOH和R'COOH,其中R和R' 为烷基)。回答下列问题: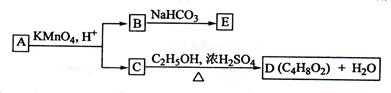
(1)直链化合物A的相对分子质量等于100,A分子中碳、氢元素的总质量分数为0.68,其余为氧元素,则A的分子式为______________
(2)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是__________。
(3)已知B与NaHCO3溶液完全反应,其物质的量之比为1:2,则在浓硫酸的催化下,B与足量的C2H5OH发生反应的化学方程式 ____________________________,
反应类型为。
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有种,其相应的结构简式是。
以五倍子为原料可制得A,A的结构简式如下图所示,试回答下列问题: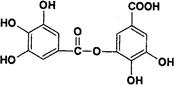
(1)A的分子式为_______________。
(2)有机化合物B在硫酸催化条件下加热发生酯化可得到A。则B的结构简式为______________。
(3)写出A与过量NaOH溶液反应的化学方程式__________________________________。
下列物质的类别与所含官能团都正确的是___________________。
选择适当试剂和操作方法除去下列物质中的少量杂质(括号内为杂质)
(1)乙烷(乙烯),试剂_______________操作方法_______________________________。
(2)苯(苯酚),试剂_________________操作方法_______________________________。