A、B、C、D四种可溶性盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是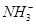 、
、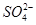 、Cl-、
、Cl-、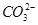 中的某一种。
中的某一种。
(1)若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色。
(2)若向(1)的四支试管中分别加盐酸,B盐溶液有沉淀产生,D盐溶液有无色无味气体逸出。
根据(1)、(2)实验事实可推断它们的化学式为:
A________、B________、C________、D________。
利用如图所示装置制备饱和氯水,探究新制饱和氯水的组成和性质。用胶头滴管将该氯水逐滴滴入盛有含酚酞的NaOH溶液的试管中,边滴边振荡,并连续观察现象,发现溶液的红色逐渐褪去得无色溶液。据此回答: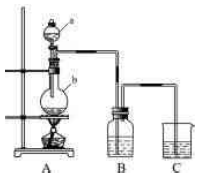
(1)仪器b的名称为,b中发生反应的离子方程式为。
(2)如何检验A装置的气密性
(3)氯水长时间放置,pH将会
(4)根据预测,实验中溶液红色褪去的原因可能有两种,请用简要的文字补充:
①氯水与NaOH反应,碱性减弱红色褪去。②。
(5)通过实验进一步探究溶液红色褪去的原因究竟是上述中的①还是②。
【实验步骤】
①取上述实验后试管内的无色溶液3 mL盛于另一支洁净的试管中;②,振荡试管。
【现象与结论】
①若,则证明溶液红色褪去的原因是①而不是②。
②若,则证明溶液红色褪去的原因是②而不是①。
(6)为了从新制氯水中制得较高浓度的HClO,可向氯水中加入的试剂是。
| A.CaCO3 | B.NaHSO3 | C.饱和 NaCl溶液 | D.Ca(OH)2 |
(7)有人提议本实验AB之间要加一个盛有饱和食盐水的除杂装置,你认为是否有必要(填“是”或“否”)______
(8)本实验有一明显的错误是,改正措施是
ⅠPM2.5是连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 |
K+ |
Na+ |
NH4+ |
SO42- |
NO3- |
Cl- |
| 浓度/mol•L-1 |
4×10-6 |
6×10-6 |
2×10-5 |
4×10-5 |
3×10-5 |
2×10-5 |
根据表中数据判断PM2.5试样的pH。
(2)NOx汽车尾气的主要污染物之一。汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
则N2和O2反应生成NO的热化学反应方程式为
(3)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
①用离子方程式表示反应器中发生的反应:
②将生成的氢气与氧气分别通入两个多孔惰性电极,KOH溶液作为电解质溶液,负极的电极反应式_ _
Ⅱ铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。
在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
(1)检验滤液B中是否还含有铁元素的方法为:(注明试剂、现象)。
(2)将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为(填代号)。
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
(3)由滤液B制备氯化铝晶体涉及的操作为:蒸发浓缩、冷却结晶、、洗涤。
(4)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为(填代号)。
I.下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。
现用该浓硫酸配制100 mL 1 mol/L的稀硫酸。可供选用的仪器有:
①胶头滴管;②烧瓶;③烧杯;④ 药匙;⑤量筒;
⑥托盘天平;⑦玻璃棒;⑧100mL容量瓶。请回答:
(1)配制稀硫酸时,上述仪器中不需要使用的有(选填序号)。
(2)经计算,配制100mL1mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为mL。
(3)下列操作会使配制的溶液浓度偏高的是()
| A.量取浓H2SO4时,俯视刻度线 |
| B.定容时,俯视容量瓶刻度线 |
| C.配制前,容量瓶中有水珠 |
| D.定容后摇匀发现液面下降,但未向其中再加水 |
II.把一定质量的镁、铝混合物投入到1mol·L-1的盐酸中,待金属完全溶解后,向溶液中加入1mol·L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示。
则:
(1)金属铝的质量为________g(2)a的取值范围是________ml。
某铝合金中含有铁、铝、镁、铜、硅。为了测定该合金中铝的含量,现设计了如下实验:
已知:Si+2NaOH+H2O=Na2 Si O3+2H2↑,H2Si O3是不溶于水的弱酸。
(1)固体A的成分是:____________,溶液M中的阴离子有:____________________
(2)步骤③中生成沉淀的离子方程式为:_____________________________________
(3)步骤④中,用到的仪器有三脚架、酒精灯以及
(4)在空气中将NaOH溶液滴入FeCl2溶液中,观察到的现象是 ,反应的化学方程式是,
(5)该样品中铝的质量分数是:_______________________________(用a、b表示)。
(6)下列因操作不当,会使测定结果偏大的是___________
| A.第①步中加入NaOH溶液不足 | B.第②步中加入盐酸不足时 |
| C.第④步中的沉淀未用蒸馏水洗涤 | D.第④步对沉淀灼烧不充分 |
(22分)现有下列九种物质:
①H2 ②铝 ③CuO ④CO2⑤H2SO4 ⑥Ba(OH)2固体⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3
(1)按物质的分类方法填写表格的空白处:
| 分类标准 |
能导电 |
非电解质 |
电解质 |
| 属于该类的物质 |
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH- H2O,该离子反应对应的化学方程式为。
H2O,该离子反应对应的化学方程式为。
(3)⑨在水中的电离方程式为,
34.2g⑨溶于水配成250mL溶液, SO42-的物质的量浓度为。
(4)少量的④通入⑥的溶液中反应的离子方程式为:。
(5)将②加入NaOH的溶液中反应的离子方程式
(6)②与⑧发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是
(填化学式),还原剂与氧化剂的物质的量之比是,当有5.4g Al发生反应时,转移电子的物质的量为。