(1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在下表中填空,表示称量过程,并在图3—2所示的游码尺上画出游码的位置(画“|”表示)。
| 砝码质量/g |
50 |
20 |
20 |
10 |
5 |
| 取用砝码情况 |
|
|
|
|
|

(2)图3—3表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量筒中的液体的体积是__________mL。
(3)用18mol•L—1的硫酸溶液配制0.5mol•L—1的硫酸溶液250mL所需的玻璃仪器为___________。
按要求完成下列问题:
(1)DDT人类合成的第一种有机氯农药,其分子结构球棍模型如图所示。请写出其结构简式;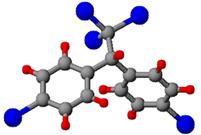
(2)用系统命名法给烃: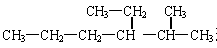 进行命名,它的名称是:;
进行命名,它的名称是:;
(3)有机物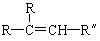 在一定条件下氧化可得产物
在一定条件下氧化可得产物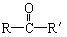 和
和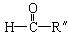 。蚂蚁跟踪信息素叶香叶醇是一种液态不饱和醇,这种醇1mol在一定条件下氧化得到产物:
。蚂蚁跟踪信息素叶香叶醇是一种液态不饱和醇,这种醇1mol在一定条件下氧化得到产物: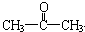 、
、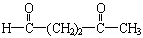 和
和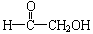 各1 mol。这种信息素的结构简式是 ___________________________________________________。
各1 mol。这种信息素的结构简式是 ___________________________________________________。
( 7分 )某学生设计了如下实验: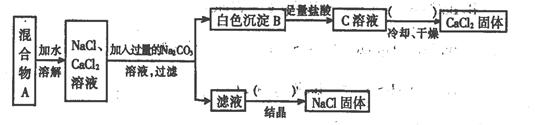
回答下列问题:
(1)该同学的实验目的是
(2)上图括号内的操作步骤均为:,所需的两种玻璃仪器是:、
(3)按此实验方案得到的NaCl固体中肯定含有(填化学式)杂质;为了解决这个问题可以向过滤得到的滤液中加入适量的;
(4)写出生成B的化学方程式:
松油醇是一种天然有机化合物,存在于芳樟油、玉树油及橙花油等天然植物精油中,具有紫丁香香气,在香料工业中用途广泛,主要用于香皂及化妆品香料和调合香精。
请写出松油醇分别与下列试剂反应所得主要有机产物的结构式(不考虑立体异构体):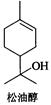
I、Br2/CC14;II、KMnO4(稀、冷溶液);
III、KMnO4/ H3O+;IV、PBr3;
V、(a) Na,(b) CH3I;VI、CH3COC1/碱。
某芳香族化合物A的分子式为C8H9OBr,其苯环上的一氯代物只有两种。A、B、C、D、E、F、G七种物质的转化关系如下图所示(图中某些生成物已略去):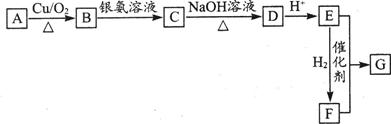
其中A、E与FeCl3溶液均不能发生显色反应,G的相对分子质量为274。
请回答下列问题:
(1)A的结构简式是。
(2)E分子所含含氧官能团的名称是、。
(3)由C生成D的化学方程式是。
(4)由E和F反应生成G的反应类型为,其化学方程式是。
(5) CH3(CH2)5CH=CH(CH2)9CHO是一种昆虫信息素。欲证明该分子中含有碳碳双键的实验方法是。
2005年诺贝尔化学奖授予法国和美国的三位科学家,以表彰他们在烯烃复分解反应研究方面作出的重要贡献。烯烃复分解反应过程被化学家描述为“交换舞伴的交谊舞”。
(I)下列图示可以被理解为烯烃复分解反应过程的是( )。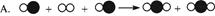

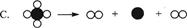

(II)烯烃复分解反应实现了在一定条件下烯烃中碳碳双键两边基团的换位。如:
又已知:两个醛分子在一定条件下可以发生加成反应: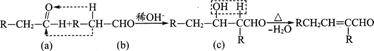
现仅以丙烯为有机原料,经过下列反应可以分别合成重要的化工原料F和K,以F和K为原料可合成一种链状高分子化合物M,其化学组成为(C12H20O4)n。
回答下列问题: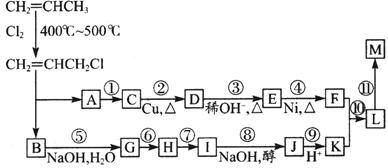
(1)反应①的反应类型是,反应⑤的反应类型是。
(2)反应⑥⑦中有一反应是与HCl加成,该反应是(填反应编号),
设计这一步反应的目的是。
(3) 物质E的结构简式为:,物质M的结构简式为:。
(4)写出下列反应的化学方程式:反应⑧:;
反应⑩:。